
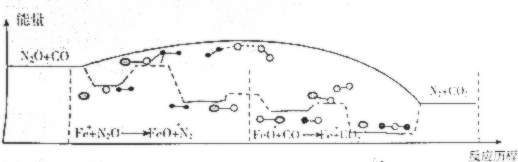
| A. | N2O与CO反应的△H<0 | |
| B. | FeO+也是该反应的催化剂 | |
| C. | Fe+使该反应的活化能减小 | |
| D. | Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为放热反应 |
分析 A、反应物的总能量高生成物的总能量,则反应是放热反应;
B、FeO+是中间产物;
C、Fe+是催化剂,降低该反应的活化能;
D、由图可知Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应,都是反应物的总能高于生成物的总能量.
解答 解:A、反应物的总能量高生成物的总能量,则反应是放热反应,所以反应的△H<0,故A正确;
B、FeO+是中间产物,而不是催化剂,故B错误;
C、Fe+是催化剂,降低该反应的活化能,所以Fe+使该反应的活化能减小,故C正确;
D、由图可知Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应,都是反应物的总能高于生成物的总能量,所以两步反应均为放热反应,故D正确;
故选B.
点评 本题考查化学反应中的能量变化及其能量的关系,注意催化剂和中间产物的判断,题目难度中等,注重基础知识的考查.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
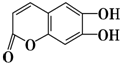 中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用.有机物M是中药狼把草的成分之一,其结构如图所示.下列叙述不正确的是( )
中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用.有机物M是中药狼把草的成分之一,其结构如图所示.下列叙述不正确的是( )| A. | M是芳香族化合物,它的分子式为C9H6O4 | |
| B. | 1 mol M最多能与3 mol Br2发生反应 | |
| C. | 1 mol M最多能与含有3 mol NaOH的溶液发生反应 | |
| D. | 在一定条件下能发生取代、加成、水解、氧化等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH的燃烧热为1452kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H>-571.6kJ/mol | |
| C. | 2CH3OH(l)+O2(g)═2CO2(g)+4H2(g)△H=-880.4kJ/mol | |
| D. | CH3COOH(aq)+NaOH(aq)═H2O(l)+CH3COONa(aq)△H=-57.3kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 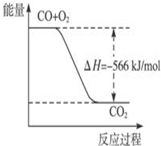 图可表示由CO生成CO2的反应过程和能量关系 | |
| B. | CO的燃烧热为566 kJ/mol | |
| C. | Na2O2(s)+CO2(s)=Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226 kJ/mol | |
| D. | CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 8min时表示正反应速率等于逆反应速率 | |
| B. | 在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 | |
| C. | 40min时改变的条件是升高温度,且正反应为放热反应 | |
| D. | 反应方程式中的x=1,30min时改变的条件是降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )| A. | 溶液中K+向电极b移动 | |
| B. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| C. | 氨气在电极a上发生氧化反应 | |
| D. | 正极的电极反应式为:O2+4e-+2H20=4OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com