
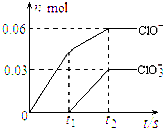
 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、反应中转移电子的物质的量是0.21mol |
| B、ClO3-的生成是由于温度升高引起的 |
| C、苛性钾溶液中KOH的质量是16.8g |
| D、氯气被还原成0.06molClO-和0.03molClO3- |


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A、①② | B、④③ | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电池工作时,电子由铝板沿导线流向铂网 |
| B、正极反应为:O2+H2O+2e-=2OH- |
| C、铂电极做成网状,可增大与氧气的接触面积 |
| D、该电池通常只需要更换铝板就可继续使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、①⑤ |
| C、②③④ | D、②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将pH=5的盐酸稀释100倍所得溶液 |
| B、c(H+)=c(OH-)=1×10-6mol/L的溶液 |
| C、由强酸、强碱等物质的量反应得到的溶液 |
| D、非电解质溶于水得到的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,1.12L 16O2和1.12L 18O2均含有0.1NA个氧原子 |
| B、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| C、能使甲基橙显红色的溶液中大量存在:Mg2+、Fe2+、Cl-、NO3- |
| D、从C(石墨)═C(金刚石);△H=+1.9kJ?mol-1,可知金刚石比石墨更稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com