
| A. | 碳酸钠固体中加少量水 | B. | 碳酸氢钠固体中加少量水 | ||
| C. | 钠与水的反应 | D. | 过氧化钠与水反应 |
科目:高中化学 来源: 题型:解答题
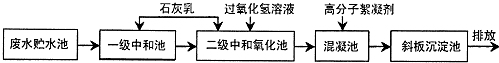
| 离子 | H+ | Cl- | Fe2+ | Fe3+ |
| 浓度(mol•L)-1 | 0.16 | 0.94 | 0.18 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
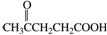 合成聚芳酯E的路线:
合成聚芳酯E的路线: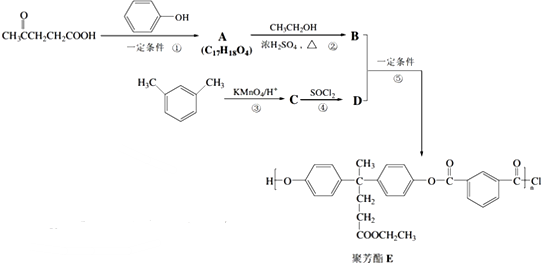
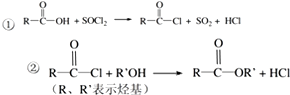
 .
. .
.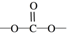 结构
结构 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H++NH4++2OH-→NH3+2H2O | |
| B. | Ba2++2OH-+SO42-+2H+→BaSO4↓+2H2O | |
| C. | 2Ba2++6OH-+2SO42-+2Fe3+→2BaSO4↓+2Fe(OH)3↓ | |
| D. | Ba2++2OH-+SO42-+NH4++H+→NH3+BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
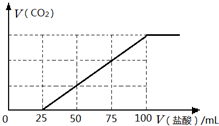 钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
钠及其化合物在生产和生活中有广泛的应用.完成下列计算:| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质本身在常温常压下不一定导电 | |
| B. | 盐酸导电所以它是电解质 | |
| C. | 酸、碱、盐是电解质 | |
| D. | 氯化钠加入水中,在水分子作用下,形成自由移动的水合离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 酸雨的PH为5.6 | |
| B. | 酸雨的形成过程发生了氧化还原反应 | |
| C. | 酸雨的主要成分为氮、硫元素的氧化物 | |
| D. | 形成酸雨的主要原因是因为雷雨天气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K值不变,平衡可能移动 | |
| B. | 平衡向右移动时,K值不一定移动 | |
| C. | K值有变化,平衡一定移动 | |
| D. | 相同条件下,同一个反应的方程式的化学计量数增大2倍,K值也增大两倍 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
下列关于电解质的叙述中,正确的是
①硫酸银在水中的溶解度很小,其溶液的导电能力很弱,所以硫酸银是弱电解质
②碳酸钙在水中的溶解度虽小,但溶解的部分全部电离,所以碳酸钙是强电解质
③氨气的水溶液导电性很好,所以它是强电解质
④水难电离,纯水几乎不导电,所以水是弱电解质
A.② B.① C.①③ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com