
| A. | H++NH4++2OH-→NH3+2H2O | |
| B. | Ba2++2OH-+SO42-+2H+→BaSO4↓+2H2O | |
| C. | 2Ba2++6OH-+2SO42-+2Fe3+→2BaSO4↓+2Fe(OH)3↓ | |
| D. | Ba2++2OH-+SO42-+NH4++H+→NH3+BaSO4↓+2H2O |
分析 加入铝片,产生H2的溶液可能为酸性溶液或者碱性溶液,若为酸性溶液则溶液含有含有离子为:H+、NH4+、Fe3+、SO42-中,有因为各溶液离子浓度相等,依据电荷守恒,可知不含三价铁离子;
若为碱性溶液,则氢离子、铵根离子、三价铁离子都不存在,溶液无阳离子,不符合题意,排除,则原溶液中含有H+、NH4+、SO42-,氢离子、铵根离子能够与氢氧根离子反应,硫酸根离子能够与钡离子反应,据此写出离子方程式.
解答 解:加入铝片,产生H2的溶液可能为酸性溶液或者碱性溶液,若为酸性溶液则溶液含有含有离子为:H+、NH4+、Fe3+、SO42-中,有因为各溶液离子浓度相等,依据电荷守恒,可知不含三价铁离子;
若为碱性溶液,则氢离子、铵根离子、三价铁离子都不存在,溶液无阳离子,不符合题意,排除,则原溶液中含有H+、NH4+、SO42-,氢离子与铵根离子离子与氢氧根离子都反应,氢离子先反应,
加入少量氢氧化钡,离子方程式:Ba2++2OH-+SO42-+2H+→BaSO4↓+2H2O;
加入过量氢氧化钡,离子方程式:Ba2++2OH-+SO42-+NH4++H+→NH3+BaSO4↓+2H2O;
故选:BD.
点评 本题考查了离子方程式的书写,准确分析溶液中所含离子成分是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 3-戊醇发生消去反应时可得2种不同的烯烃 | |
| B. | 聚合物 可由单体CH3CH=CH2和CH2=CH2加聚制得 可由单体CH3CH=CH2和CH2=CH2加聚制得 | |
| C. | 醇在Cu/△条件下都能氧化成醛 | |
| D. | 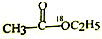 在酸性条件下水解产物是 在酸性条件下水解产物是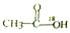 和C2H5OH 和C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgO、Al2O3熔点高,都可用于制作耐火材料 | |
| B. | 氨气显碱性,可用碱石灰或无水CaCl2干燥 | |
| C. | 氢氟酸具有强酸性,可用于雕刻玻璃 | |
| D. | 铜的活动性比铁弱,可在海轮外壳上装铜块以减缓海轮腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Na+、Cl-、NO3- | B. | Fe3+、Ba2+、Cl-、I- | ||
| C. | Na+、NH4+、SO42-、OH- | D. | K+、Ca2+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
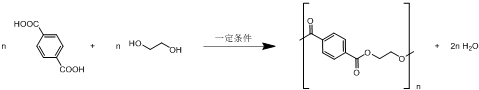 .
.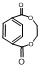 .
.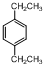 .
.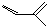 ,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物
,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物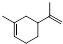 、
、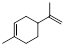 .
.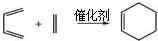
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:填空题
化学学习中要注意对过程的分析,按要求回答下列问题:
(1)向石蕊试剂中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是 、 。
(2)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液到中性,写出发生反应的离子方程式 ;在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com