
| A. |  高炉炼铁 | B. |  火箭发射 | C. | 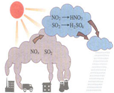 酸雨的形成 | D. |  丁达尔效应 |
分析 A.金属的冶炼是金属从化合态变为游离态的过程,属于化学变化;
B.火箭发射涉及燃料的燃烧;
C.酸雨主要是人为地向大气中排放大量酸性物质造成的;
D.丁达尔效应是胶粒对光线的散射作用形成的.
解答 解:A.高炉炼铁涉及Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2等反应,属于化学变化,故A错误;
B.火箭发射涉及燃料的燃烧,涉及化学变化,故B错误;
C.酸雨分两种,硫酸型与硝酸型,硫酸型SO2+H2O=H2SO3、2H2SO3+O2=2H2SO4,硝酸型2NO+O2=2NO2、3NO2+H2O=2HNO3+NO,故C错误;
D.丁达尔效应是胶粒对光线的散射作用形成的,不涉及化学变化,故D正确;
故选D.
点评 本题考查物理变化与化学变化的区别与联系,涉及化学反应与生活、生产的考查,为高频考点,侧重于学生的分析能力的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 用硫磺熏蒸使银耳增白 | |
| B. | 用废旧皮革生产药用胶囊可以提高原子利用率 | |
| C. | 用明矾对自来水进行杀菌消毒 | |
| D. | 限制使用一次性塑料制品的主要目的是防止形成“白色污染” |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H++NH4++2OH-→NH3+2H2O | |
| B. | Ba2++2OH-+SO42-+2H+→BaSO4↓+2H2O | |
| C. | 2Ba2++6OH-+2SO42-+2Fe3+→2BaSO4↓+2Fe(OH)3↓ | |
| D. | Ba2++2OH-+SO42-+NH4++H+→NH3+BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质本身在常温常压下不一定导电 | |
| B. | 盐酸导电所以它是电解质 | |
| C. | 酸、碱、盐是电解质 | |
| D. | 氯化钠加入水中,在水分子作用下,形成自由移动的水合离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 酸雨的PH为5.6 | |
| B. | 酸雨的形成过程发生了氧化还原反应 | |
| C. | 酸雨的主要成分为氮、硫元素的氧化物 | |
| D. | 形成酸雨的主要原因是因为雷雨天气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | A 探究铁发生吸 氧腐蚀 | B探究碳和硅金 属性的强弱 | C制取并收集氨气 | D制取并探究乙 炔的性质 |
实验方案 | 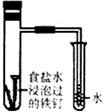 | 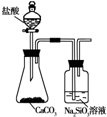 | 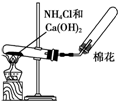 | 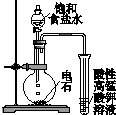 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K值不变,平衡可能移动 | |
| B. | 平衡向右移动时,K值不一定移动 | |
| C. | K值有变化,平衡一定移动 | |
| D. | 相同条件下,同一个反应的方程式的化学计量数增大2倍,K值也增大两倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:填空题
在一定温度下,有a盐酸 b、硫酸 c、醋酸三种酸:
(1)当其物质的量浓度相同时,c(H+)由大到小的顺序是 。(填序号,下同)
(2)同物质的量浓度的三种酸,中和相同物质的量的NaOH溶液所需酸的体积由大到小的顺序是 。
(3)若三者c(H+)相同时,物质的量浓度大小的顺序是 。
(4)若三者c(H+)相同,体积也相同时,分别放入足量的且同样的锌,相同状况下产生气体的体积由大到小的顺序是 ,生成同体积的气体所需时间由大到小的顺序是 。
(5)将c(H+)相同的三种酸均加水稀释到原来的100倍时,c(H+)由大到小的顺序是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com