
| A��������Һ������Ũ�ȵĹ�ϵ���㣺c��H+��=c��OH-��+c��CH3COO-�� |
| B��0.10mol/L��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c��OH-����С |
| C��CH3COOH��Һ�м�������CH3COONa���壬ƽ�������ƶ� |
| D��������pH=2��CH3COOH��Һ��pH=12��NaOH��Һ�������Ϻ���Һ��pH��7 |


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CO2�к�����HCl���壬���ñ����Ȼ�����Һ���� | ||
B��ij��Һ
| ||
| C��CO2�к�����SO2���壬���ñ���̼������Һ���� | ||
D��ij��Һ
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH3-CH=CH-CH2-CH3 |
B��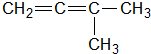 |
C�� |
D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
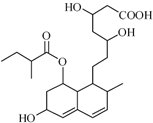 �շ���͡��һ�ֵ���Ѫ֬��ҩ���ṹ��ʽ��ͼ��ʾ��δ��ʾ����ռ乹�ͣ������й����շ���͡������������ȷ���ǣ�������
�շ���͡��һ�ֵ���Ѫ֬��ҩ���ṹ��ʽ��ͼ��ʾ��δ��ʾ����ռ乹�ͣ������й����շ���͡������������ȷ���ǣ�������| A������FeCl3 ��Һ������ɫ��Ӧ |
| B������ʹ����KMnO4 ��Һ��ɫ |
| C���ܷ����ӳɡ�ȡ������ȥ��Ӧ |
| D��1 mol ������������1 mol NaOH ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
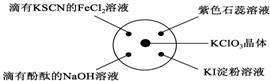 ��֪��KClO3+6HCl��Ũ���TKCl+3Cl2��+3H2O����ͼ��ʾ���������Լ��ֱ�����������е���Ӧλ�ã�ʵ��ʱ��Ũ�������KClO3�����ϣ����ñ�����Ǻã��±�����ʵ������ó��Ľ�����ȫ��ȷ���ǣ�������
��֪��KClO3+6HCl��Ũ���TKCl+3Cl2��+3H2O����ͼ��ʾ���������Լ��ֱ�����������е���Ӧλ�ã�ʵ��ʱ��Ũ�������KClO3�����ϣ����ñ�����Ǻã��±�����ʵ������ó��Ľ�����ȫ��ȷ���ǣ������� | ѡ�� | ʵ������ | ���� |
| A | ����KSCN��FeCl2��Һ��� | Cl2���л�ԭ�� |
| B | ���з�̪��NaOH��Һ��ɫ | Cl2�������� |
| C | ʯ����Һ�ȱ�����ɫ | Cl2����Ư���� |
| D | KI������Һ���� | Cl2���������� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com