
【题目】由反应物 X 分别转化为 Y 和 Z 的能量变化如图所示。下列说法正确的是( )
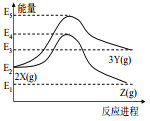
A.由 X→Z 反应的 ΔH<0 B.由 X→Y 反应的 ΔH=E5-E2
C.增大压强有利于提高 Y 的产率 D.升高温度有利于提高 Z 的产率
科目:高中化学 来源: 题型:
【题目】作催熟剂的物质除乙烯外,还有氯酸镁。实验室制备少量氯酸镁晶体【Mg(ClO3)2·6H2O】的流程如下:
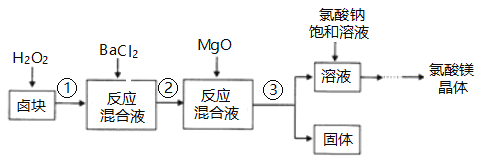

(1)步骤③的操作名称是___________,该步分离出的固体中含有多种成分,任写出一种成分的化学式____________________。
(2)用双氧水溶解卤块,H2O2的主要作用是___________________。
(3)加入饱和氯酸钠溶液发生的主要反应的反应类型是_________________(填四大基本反应类型)。
(4)若卤块中MgCl2·6H2O含量为81.2%,用10L饱和氯酸钠溶液(其中溶质利用率为90%),理论上可以制得氯酸镁晶体的质量是___________(用带a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实,不能用勒夏特列原理解释的是( )
A.溴水中有下列平衡Br2+H2O![]() HBr + HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr + HBrO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g)![]() H2(g)+I2(g),平衡体系增大压强可使颜色变深
H2(g)+I2(g),平衡体系增大压强可使颜色变深
C.反应CO+NO2![]() CO2+NO △H<0,升高温度可使平衡向逆反应方向移动
CO2+NO △H<0,升高温度可使平衡向逆反应方向移动
D.合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2、CS2、COS是由C、O、S三种元素形成的结构相似的化合物。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是_____________(填序号)
A.亚硫酸溶液加入Na2CO3溶液中,产生气泡
B.氧化性:浓H2SO4>H2CO3
C.CS2中碳元素为+4价,硫元素为—2价
D.SO2有较强还原性,而CO2无还原性
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。
① 羰基硫的结构式为:________________。沸点:CO2_________COS(填“大于”或“小于”),说明原因_____________________。
②下列有关羰基硫的推测肯定不正确的是_________________
A.COS分子中,所有原子都满足8电子的稳定结构
B.COS分子是含有极性键的非极性分子
C.COS分子中三个原子处于同一直线上
D.COS可能在O2中燃烧
③ 羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下图:

已知A是一种盐,则A的化学式为________;气体单质a为____________________.
(3)在恒容密闭容器中,CO和H2S混合加热生成羰基硫的反应为CO(g)+H2S(g)![]() COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
COS(g)+H2(g),反应前CO和H2S的物质的量均为10mol,平衡后CO的物质的量为8mol,回答下列问题:
①升高温度,H2S浓度增加,表明该反应是__________________反应(填“放热”或“吸热”)。
②平衡时,继续通入CO10mol和H2S10mol,一段时间后再次达到平衡,此时H2S的转化率_____(填“增大”“减小”或“不变”)
(4)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是____________
A.容器内气体密度保持不变
B.CO、H2S、COS、H2的浓度均不再变化
C.c(H2)=c(H2S)
D.v(H2)正=v(H2S)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下,将一盛有等体积NO、NO2的试管倒立在水槽中,充分反应后,下列叙述不正确的是(设试管中的溶质不往试管外扩散)( )
A. 溶液体积占试管容积的2/3
B. 此反应中水既不作氧化剂也不作还原剂
C. 试管内溶液中溶质的物质的量浓度为1/22.4mol/L
D. 若将试管中的气体改为氯化氢或氨气,则水充满试管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图中的曲线是表示其他条件一定时,2NO+O2![]() 2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是
2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是

A. a点 B. b点 C. c点 D. d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1molNa2SO4溶解在多少毫升水中,才能使每100个水分子中含有一个Na+离子 ( )
A.200mL B.20mL C.360mL D.36mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究大气中含硫化合物和含碳化合物的转化对环境保护具有重要意义。
(1)SO2的大量排放会引起严重的环境问题是 ,潮湿条件下,写出大气中SO2转化为HSO3-的方程式 ;
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42-,两步反应的能量变化示意图如下:

1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式为 ;
(3)SO2是工业制硫酸的原料之一,一定温度下,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g),过程中测定的部分数据见下表:
2SO3(g),过程中测定的部分数据见下表:
时间/min | n(SO2)/mol | n(O2)/mol |
0 | 0.10 | 0.05 |
4 | 0.04 | 0.02 |
6 | 0.02 | |
8 | 0.01 |
①反应在0-4min内的平均速率为v(SO2)= ;
②此温度下该反应的化学平衡常数K= ;
③8min时,维持温度不变,向反应容器中再通入0.02mol SO2(g)和0.01mol O2(g),重新达到平衡时混合气体中SO2的百分含量将 (填“减小”、“增大”或“不变”)。
(4)科学家用氮化镓材料与铜组装如下图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4的反应。

写出铜电极表面的电极反应式 ,为提高该人工光合系统的工作效率,可向装置中加入少量 (填“盐酸”或“硫酸”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com