
【题目】使用胆矾(CuSO45H2O)配制0.1 molL-1的硫酸铜溶液,正确的操作是( )
A. 将胆矾加热除去结晶水后,称取16g溶解在1 L水中
B. 称取25 g胆矾溶于水,然后将此溶液稀释至1 L
C. 称取25 g胆矾溶解在1 L水里
D. 将16 g胆矾溶于水,然后将此溶液稀释至1 L
科目:高中化学 来源: 题型:
【题目】已知1,2-二氯乙烷常温下为无色液体,沸点为83.5 ℃,密度为1.23 g/mL,难溶于水,易溶于醇、醚、丙酮等有机溶剂。乙醇的沸点为78.5 ℃。某化学课外活动小组为探究1,2-二氯乙烷的消去反应,设计了如下实验装置。请回答下列问题:

(1)将导气管末端插入盛水的C试管中,用酒精灯加热(或用手捂)装置A中大试管,若__________现象,且移开酒精灯(或松开手)一会儿,导气管中出现________,则证明装置气密性良好。
(2)向装置A中先加入1,2二氯乙烷和NaOH的乙醇溶液,再加碎瓷片,碎瓷片的作用是__。
(3)为了使反应在75℃左右进行,常用的加热方法是________________,其优点是__________。
(4)与装置A中大试管相连接的长玻璃管的作用是____________,装置B的作用是______。
(5)为证明1,2-二氯乙烷已发生消去反应,则C中应装____________,现象是_______________,装置A中发生反应的化学方程式为:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种短周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙3种分子中含有相同数目的质子,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图:

下列说法正确的是( )
A. C与A形成的常见化合物是同主族元素同类型化合物中沸点最低的
B. B是元素周期表中原子半径最小的元素
C. D的最高价氧化物的水化物一定是一种强酸
D. C的单质可以与D的氢化物发生置换反应生成D的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)B的氢化物的分子空间构型是 ,其中心原子采取 杂化。
(3)写出化合物AC2的电子式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为 。
(4)E的核外电子排布式是 ,ECl3形成的配合物的化学式为 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述中正确的是( )
A. 分子总数为NA的二氧化硫和二氧化碳混合气体中含有的原子数为3NA
B. 任何条件下,20 L 氧气含有的分子数都不可能为NA
C. 在标准状况下,2 g氖气含有NA个氖原子
D. 物质的量相等的任何气体中都含有相同的原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
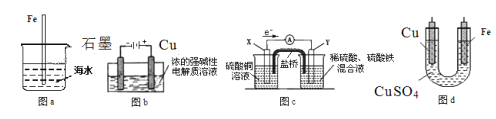
A. 图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B. Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图b所示,石墨电极上产生氢气,铜电极发生氧化反应
C. 如图c,盐桥的作用是传递电子以维持电荷平衡,Fe3+经过盐桥进入左侧烧杯中
D. 如图d铁上镀铜,铁应与外加电源负极相连,一段时间后CuSO4溶液浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 氯气通入水中: Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 向苯酚浊液中滴加Na2CO3溶液:2C6H5OH+CO32-=2C6H5O-+H2O+CO2↑
C. 向偏铝酸钠溶液中加入NaHCO3溶液: AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-
D. 碳酸氢铵溶液中加入足量NaOH溶液共热: NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积均为1.0 L的恒容密闭容器中仅发生反应:CH3OH(g)+CO(g)![]() CH3COOH(g) ΔH<0。下列说法正确的是( )
CH3COOH(g) ΔH<0。下列说法正确的是( )

A. 达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为3∶4
B. 达平衡时,容器Ⅱ中![]() 比容器Ⅰ中的大
比容器Ⅰ中的大
C. 达平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
D. 达平衡时,容器Ⅰ中CH3OH转化率与容器Ⅲ中CH3COOH转化率之和小于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰氧基胡椒酚乙酸酯(F)具有抗氧化性、抗肿瘤作用,其合成路线如下:
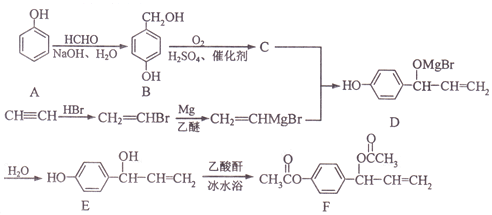
已知:RMgBr![]()
(1)化合物F中含氧官能团的名称为______。
(2)A-B的反应类型为_______。
(3)化合物C的结构简式为______。
(4)1mol化合物E与足量乙酸酐[(CH3CO)2O]反应,除F外另一产物的物质的量为_______。
(5)写出同时满足下列条件的E的一种同分异构体的结构简式:________。
①能与FeCl3溶液发生显色反应; ②能发生银镜反应;
③核磁共振氢谱显示有4种不同化学环境的氢,其峰面积比为6:2:1:1。
(6)请以甲苯和乙醛为原料制备![]() ,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)_______________
,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com