
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol?L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
| A、2p2<p3 |
| B、a+b=184.8 |
| C、2c1<c3 |
| D、a1+a3>1 |


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| A、35.5:108 |
| B、l:2 |
| C、108:35.5 |
| D、8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质A、B的转化率之比为a:b | ||
| B、当v正(A)=2v逆(B)时,可确定反应达到平衡 | ||
C、起始时刻和达到平衡后容器中的压强比为(a+b):(a+b-
| ||
| D、若起始时放入2a mol A和2b mol B,则达到平衡时生成2n mol C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 压强 | MPa | 15.2 | 20.3 | 30.4 | 40.5 |
| 温 度 | 400℃ | 32.8 | 38.8 | 48.2 | 55.4 |
| 450℃ | 22.4 | 27.5 | 35.9 | 42.9 | |
| 500℃ | 14.9 | 18.8 | 25.8 | 31.9 | |
| 550℃ | 9.90 | 12.8 | 18.2 | 23.2 |
| C(NH3) |
| C(N2)1/2?c(H2)3/2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水,用湿润的红色石蕊试纸放在试管口检验 |
| B、将固体加热,用湿润的红色石蕊试纸放在试管口检验 |
| C、加入NaOH溶液,加热,用湿润的红色石蕊试纸放在试管口检验 |
| D、加入NaOH溶液,加热,滴入无色酚酞 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷和乙烯 |
| B、甲烷和丙烯 |
| C、乙烷和乙烯 |
| D、乙烷和丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
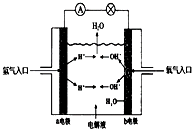
| A、a电极是负极 |
| B、b电极上发生氧化反应 |
| C、氢氧燃料电池是一种具有应用前景的绿色电源 |
| D、氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com