
【题目】控制变量是科学研究的重要方法。相同质量的铝与足量1 mol·L-1盐酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是( )
选项 | 铝的状态 | 实验温度/℃ |
A | 片状 | 20 |
B | 片状 | 30 |
C | 粉末 | 20 |
D | 粉末 | 30 |
A.AB.BC.CD.D
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】某烃可以用通式CnH2n来表示,下列有关此烃的说法正确的是
A. 分子中一定有C=C双键 B. 分子中一定没有C=C双键
C. 分子可能有C=C双键 D. 分子中不可能只含单键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g)![]() 2C1NO(g),
2C1NO(g),
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
① 2NO2(g)+NaC1(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
② 4NO2(g)+2NaC1(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③ 2NO(g)+C12(g)![]() 2C1NO(g) K3
2C1NO(g) K3
则K1,K2,K3之间的关系为K3=______________。
(2)已知几种化学键的键能数据如下表(亚硝酸氯的结构为Cl-N=O):

则2NO(g)+C12(g)![]() 2C1NO(g)反应的△H和a的关系为△H=________kJ/mol。
2C1NO(g)反应的△H和a的关系为△H=________kJ/mol。
(3)在1L的恒容密闭容器中充入2molNO(g)和1molC12(g),在不同温度下测得c(C1NO)与时间的关系如图A:
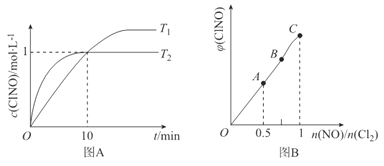
① 由图A可判断T1 ________T2,该反应的△H________0 (填“>”“<”或“=”)。
② 反应开始到10min时NO的平均反应速率v(NO)=____________mol/(L·min)。
③ T2时该反应的平衡常数K=____________。
(4) 一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是________点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢核磁共振谱是根据不同化学环境的氢原子在谱中给出的信号不同来确定有机物分子中氢原子种类的。下列有机物分子中,在氢核磁共振谱中只给出一种信号的是( )
A. 丙烷 B. 新戊烷 C. 正丁烷 D. 异丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生如下反应:mA(g)+nB(g) ![]() pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的![]() ,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
A. ![]() B. 平衡向逆反应方向移动
B. 平衡向逆反应方向移动
C. A的转化率不变 D. C的体积分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在C2H2、C6H6、C2H4O组成的混合物中,已知氧元素的质量分数为16%,则混合物中碳元素的质量分数是 ( )
A. 92.3% B. 75.7% C. 65% D. 86%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个化学过程的示意图。
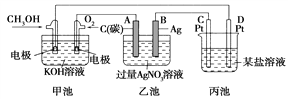
(1)图中甲池是________装置(填“电解池”或“原电池”),其中OH-移向________极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式: _______________________。
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为________极(填“A”或“B”),并写出此电极的反应式:______________。
(4)乙池中总反应的离子方程式:____________。
(5)常温下,当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是________(若此时乙池中溶液的体积为500 mL);此时丙池某电极析出1.60 g某金属,则丙中的某盐溶液可能是________(填序号)。
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com