
 2C��g������H<0��
2C��g������H<0��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
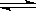 eC(g )+dD (g) ��H<0������֤���÷�Ӧһ���ﵽƽ��״̬����
eC(g )+dD (g) ��H<0������֤���÷�Ӧһ���ﵽƽ��״̬�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 z C(g)��ƽ��ʱ���A��Ũ��Ϊ 0.5 mol/L�������¶Ȳ��䣬���������ݻ�ѹ����ԭ����1/2���ٴ�ƽ��ʱ���A��Ũ��Ϊ 0.8mol/L�������ж���ȷ���ǣ� ��
z C(g)��ƽ��ʱ���A��Ũ��Ϊ 0.5 mol/L�������¶Ȳ��䣬���������ݻ�ѹ����ԭ����1/2���ٴ�ƽ��ʱ���A��Ũ��Ϊ 0.8mol/L�������ж���ȷ���ǣ� ��| A��x+y ��z | B��ƽ��������Ӧ�����ƶ� |
| C��B�����ʵ������� | D��C������������ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3C��g��+2D��g�����ﵽƽ��״̬����
3C��g��+2D��g�����ﵽƽ��״̬�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
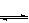 2SO3�����ﵽƽ�⡣��������У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp%������������SO2��ת����
2SO3�����ﵽƽ�⡣��������У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp%������������SO2��ת����| A������p% | B������p% | C��С��p% | D�����ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(g) + H2(g)����H=" -Q" kJ��mol-1��Q>0������֪�ﵽƽ��ʱ��COΪ0.12mol���Իش�
CO(g) + H2(g)����H=" -Q" kJ��mol-1��Q>0������֪�ﵽƽ��ʱ��COΪ0.12mol���Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 SiF4(g)+ 2H2O(g) ��H =��148.9 kJ��mo1��1
SiF4(g)+ 2H2O(g) ��H =��148.9 kJ��mo1��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
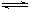 nZ(g)��R(g)�ﵽƽ��ʱ��������Ӧ��������и�����Ũ�Ⱦ�����һ����X��ת���ʲ��䣬��֪t��ʱ�÷�Ӧ��K=1����X��ת����Ϊ
nZ(g)��R(g)�ﵽƽ��ʱ��������Ӧ��������и�����Ũ�Ⱦ�����һ����X��ת���ʲ��䣬��֪t��ʱ�÷�Ӧ��K=1����X��ת����Ϊ| A��80�� | B��65�� | C��45�� | D��37�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3�Ѵ�ƽ��״̬����___ _____
2NH3�Ѵ�ƽ��״̬����___ _____ һ��ʱ������ѹǿ���ٱ仯
һ��ʱ������ѹǿ���ٱ仯�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com