
【题目】已知HA的酸性强于HB的酸性。25℃时,用NaOH固体分别改变物质的量浓度均为0.1molL-l的HA溶液和HB溶液的pH(溶液的体积变化忽略不计),溶液中A-、B-的物质的量浓度的负对数与溶液的pH的变化情况如图所示。下列说法正确的是

A.曲线I表示溶液的pH与-lgc(B-)的变化关系
B.![]()
C.溶液中水的电离程度:M>N
D.N点对应的溶液中c(Na+)>Q点对应的溶液中c(Na+)
【答案】B
【解析】
A.HA的酸性强于HB的酸性,则Ka(HA)>Ka(HB),当-1gc(A-)=-1gc(B-)时c(A-)=c(B-),c(HA)=c(HB),则c(H+)越大,pH越小,Ka越大,所以曲线II表示pH与-1gc(B-)的关系,故A错误;
B.对于HB,取点(10,2),则c(H+)=10-10mol/L,c(B-)=10-2mol/L,则Ka(HB)=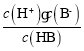 =
=![]() ,同理对于HA,取点(8,2),则c(H+)=10-8mol/L,c(A-)=10-2mol/L,则Ka(HA)=
,同理对于HA,取点(8,2),则c(H+)=10-8mol/L,c(A-)=10-2mol/L,则Ka(HA)=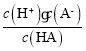 =
=![]() ,所以Ka(HA):Ka(HB)=100,故B正确;
,所以Ka(HA):Ka(HB)=100,故B正确;
C.M点和N点溶液中c(A-)=c(B-),溶液pH越大,水的电离程度越大,所以水的电离程度M<N,故C错误;
D.对于N点溶液,存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(B-),对于Q点溶液,存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(A-),N点和Q点溶液pH相同,则两溶液中c(H+)和c(OH-)分别相等,但c(B-)<c(A-),则N点对应的溶液中c(Na+)<Q点对应的溶液中c(Na+),故D错误;
故选:B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氯气是现代工业的重要原料,将氯化氢转化为氯气的技术成为科学研究的热车点,回答下列问题:
(1)Deacon发明的直接氧化法为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。可按下列催化过程进行:
Ⅰ.CuCl2(s)=CuCl(s)+![]() Cl2(g) ΔH1=+83kJ·mol-1
Cl2(g) ΔH1=+83kJ·mol-1
Ⅱ.CuCl(s)+![]() O2(g)=CuO(s)+
O2(g)=CuO(s)+![]() Cl2(g) ΔH2=-20kJ·mol-1
Cl2(g) ΔH2=-20kJ·mol-1
Ⅲ.4HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ΔH3
反应Ⅰ能自发进行的条件是___。利用ΔH1和ΔH2计算ΔH3时,还需要利用反应___的ΔH。
(2)如图为刚性容器中,进料浓度比c(HCl):c(O2)分别等于1:1、4:1、7:1时HCl平衡转化率随温度变化的关系:

可知反应平衡常数K(400℃)__K(500℃)(填“大于”或“小于”)。设容器内初始压强为p0,根据进料浓度比c(HCl):c(O2)=4:1的数据,计算400℃时容器内的平衡压强=___(列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl):c(O2)过低、过高的不利影响分别是___。
(3)已知:氯气与NaOH溶液反应可生成NaClO3。有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-=ClO2-+Cl-
Ⅱ.ClO2-+ClO-=ClO3-+Cl-
常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:___。
(4)电解NaClO3水溶液可制备NaClO4,写出阳极反应式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国Lawrece Liermore国家实验室(LINL)成功地在高压下将![]() 转化为具有类似
转化为具有类似![]() 结构的原子晶体,下列关于
结构的原子晶体,下列关于![]() 的原子晶体说法,正确的是:
的原子晶体说法,正确的是:
A. ![]() 的原子晶体和分子晶体互为同分异构体
的原子晶体和分子晶体互为同分异构体
B. 在一定条件下,![]() 原子晶体转化为
原子晶体转化为![]() 分子晶体是物理变化
分子晶体是物理变化
C. ![]() 的原子晶体和
的原子晶体和![]() 分子晶体具有相同的物理性质和化学性质
分子晶体具有相同的物理性质和化学性质
D. 在![]() 的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应[Cu(OH)2悬浊液用于检验反应产物]。
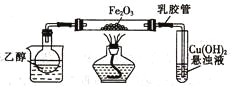
(1)组装好仪器后必须进行的操作是____________________。
(2)为快速得到乙醇气体,可采取的方法是_______________________;
若实验时小试管中的溶液已经开始发生倒吸,应采取的措施是_________(填字母)。
A.取下小试管 B.移去酒精灯 C.将导管从乳胶管中取下 D.以上都可以
(3)乙醇被氧化的产物是__________________(写结构式)。
(4)若M的成分为FexOy,用CO还原法定量测定其化学组成。称取a g M样品进行定量测定,实验装置和步骤如下:
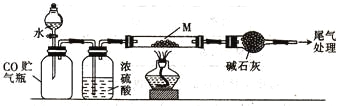
①组装仪器 ②点燃酒精灯 ③加入试剂 ④打开分液漏斗活塞 ⑤检查气密性 ⑥停止加热 ⑦关闭分液漏斗活塞 ⑧称重
ⅰ.正确的操作顺序是__________(填字母)。
a.①⑤④③②⑥⑦⑧ b.①③⑤④②⑦⑥⑧
c.①⑤③④②⑥⑦⑧ d.①③⑤②④⑥⑦⑧
ⅱ.尾气处理的方法是____________。若测得碱石灰增重b g,则x:y=______(用含有a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y和Z组成的一种化合物可有效灭杀新型冠状病毒,它的结构式为: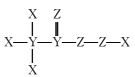 。向W的一种钠盐水溶液中通入YZ2气体,产生沉淀的质量m与通入YZ2气体的体积V的关系如图所示。下列说法正确的是
。向W的一种钠盐水溶液中通入YZ2气体,产生沉淀的质量m与通入YZ2气体的体积V的关系如图所示。下列说法正确的是
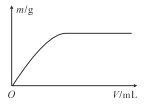
A.氢化物的熔点一定是:Y<Z
B.最高价氧化物对应水化物的酸性:Y>W
C.X、Y、Z三种元素只能组成一种化合物
D.工业上常用热还原法冶炼单质W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为元素周期表中短周期的一部分,下列关于Y、Z、M的说法正确的是 ( )

A.电负性:![]()
B.离子半径:![]()
C.![]() 分子中各原子的最外层均满足8电子稳定结构
分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子的最外层电子排布图为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.28g晶体硅中含有NA个Si-Si键
B.叠氮化铵(NH4N3)发生爆炸反应:NH4N3=2N2![]() +2H2
+2H2![]() ,当产生标准状况下22.4L气体时,转移电子的数目为NA
,当产生标准状况下22.4L气体时,转移电子的数目为NA
C.pH=1的H3PO4溶液中所含H+的数目为0.1NA
D.200mL1mol/LAl2(SO4)3溶液中A13+和SO42-的数目总和是NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列有关叙述中不正确的是( )

A.可与NaOH和Na2CO3溶液发生反应
B.1mol该有机物最多与7molH2发生反应
C.1mol该有机物可以与4molBr2发生反应
D.该有机物分子中至少有17个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S是石油化工行业广泛存在的污染性气体,但同时也是重要的氢源和硫源,工业上可以采取多种方式处理。
Ⅰ.干法脱硫
(1)已知H2S的燃烧热为akJmol-1 ,S的燃烧热为bkJmol-1 ,则常温下空气直接氧化脱除H2S的反应:2H2S(g)+O2(g)=2S(s)+2H2O(l) △H=______kJmol-1 。
(2)常用脱硫剂的脱硫效果及反应条件如下表,最佳脱硫剂为_________。
脱硫剂 | 出口硫(mg·m-3) | 脱硫温度(℃) | 操作压力(MPa) | 再生条件 |
一氧化碳 | <1.33 | 300~400 | 0~3.0 | 蒸气再生 |
活性炭 | <1.33 | 常温 | 0~3.0 | 蒸气再生 |
氧化锌 | <1.33 | 350~400 | 0~5.0 | 不再生 |
锰矿 | <3.99 | 400 | 0~2.0 | 不再生 |
Ⅱ.热分解法脱硫
在密闭容器中,充入一定量的H2S气体,发生热分解反应H2S(g)![]() 控制不同的温度和压强进行实验,结果如图(a)。
控制不同的温度和压强进行实验,结果如图(a)。
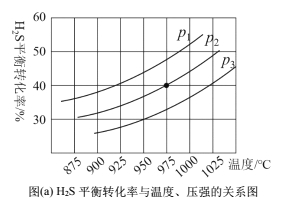
(3)图(a)中压强关系p1、p2、p3由大到小的顺序为______,该反应为____(填“吸热”或“放热”)反应,若要进一步提高H2S的平衡转化率,除了改变温度和压强外,还可以采取的措施有_______。
(4)压强为p、温度为975℃时,![]() 的平衡常数K=0.04,则起始浓度c=______molLˉ1,若向容器中再加入1molH2S气体,相同温度下再次达到平衡时,K_____0.04(填“>”1 “<”或“=”)。
的平衡常数K=0.04,则起始浓度c=______molLˉ1,若向容器中再加入1molH2S气体,相同温度下再次达到平衡时,K_____0.04(填“>”1 “<”或“=”)。
Ⅲ.间接电解法脱硫
间接电解法是通过FeCl3溶液吸收并氧化H2S气体,将反应后溶液通过电解再生,实现循环使用,该法处理过程如下图(b)。
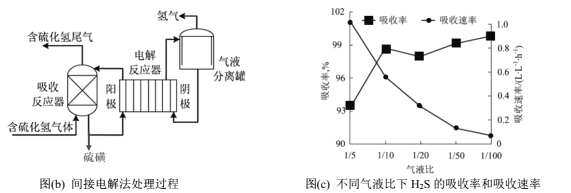
(5)电解反应器总反应的离子方程式为________。
(6)气液比为气体与液体的流速比,吸收反应器内液体流速固定。测定吸收器中相同时间内不同气液比下H2S的吸收率和吸收速率,结果如图(c)所示,随着气液比减小,H2S的吸收速率逐渐降低,而吸收率呈上升趋势的原因为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com