
【题目】在常温下,将下列物质投入足量稀盐酸中,能产生气体且有金属不溶物残留的是( )
A.黄铜 B.纯铁 C.碳酸钙 D.碳素钢
科目:高中化学 来源: 题型:
【题目】(1)现有下列物质:①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦ 蔗糖 其中属于电解质的是(填序号)___________,
(2)写出Al2(SO4)3的电离方程式:___________________,
(3)写出NaHSO3(aq) 与稀盐酸反应的离子方程式:_____________________,
(4)胶体是一种常见的分散系,回答下列问题:
①向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为__________________。
②向Fe(OH)3胶体中加入K2SO4饱和溶液,由于SO42-的作用,使胶体形成了沉淀,这个过程叫做胶体的_______。
③区分胶体和溶液常用的方法叫做__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁可用作燃料的节能消烟剂、抗爆剂等。实验室制备二茂铁装置示意图如图一
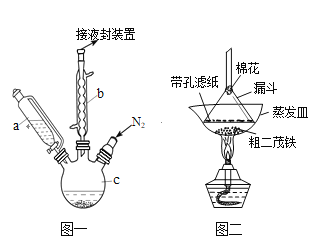
已知:①二茂铁熔点是173℃,在100℃时开始升华;沸点是249℃。
②制备二茂铁的反应原理是:2KOH+FeCl2+2C5H6= Fe(C5H5)2+2KCl+2H2O
实验步骤为:
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(C5H6, 密度为0.95g/cm3),搅拌;
③将6.5g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25mL装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入分液漏斗中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的名称是________________________.
(2)步骤①中通入氮气的目的是____________________________________________________.
(3)仪器c的适宜容积应为(选编号):_________
①100mL ②250mL ③500mL
(4)步骤⑤用盐酸洗涤的目的是__________________________________________________
(5)步骤⑦是二茂铁粗产品的提纯,该过程在图二中进行,其操作名称为_________;该操作中棉花的作用是______________________________________________________.
(6)为了确认得到的是二茂铁,还需要进行的一项简单实验是__________________________;若最终制得纯净的二茂铁4.3g,则该实验的产率为____________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生物体内,某些重要化合物的元素组成及相互关系十分密切。请据右图
分析完成下列问题。

(1)图中X、Y分别代表何种元素?X ,Y 。
(2)请在B下面的括号内填写该类物质的另外三种功能。
(3)B类物质有多种不同功能,究其原因是因为A类物质内的 不同。
(4)细胞内遗传信息的携带者是图中的 物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用下图所示的装置,用环己醇制备环己烯。
已知: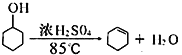
相对分子质量 | 密度/g cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 82 | 0.81 | -103 | 83 | 难溶于水 |
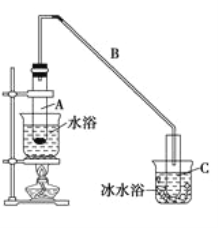
(1)制备粗品
将12.5 mL环己醇与1mL浓硫酸加入试管A中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①在试管中混合环已醇和浓硫酸操作时,加入药品的先后顺序为______________________。
②如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是_________(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
③将试管C置于冰水中的目的是_______________________________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。向粗品中加入饱和食盐水,振荡、静置、分层,环己烯在_______层(填“上”或“下”),分液后用________(填字母)洗涤。
a.酸性KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将提纯后的环己烯按如图所示装置进行蒸馏。图中仪器a 的名称是_______________,实验中冷却水从______(填字母)口进入。蒸馏时要加入生石灰,目的是__________________________。
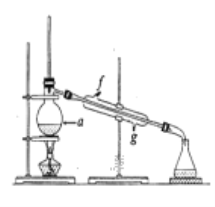
(3)若在制备粗品时环已醇随产品一起蒸出,则实验制得的环己烯精品质量_______(填“高于”、“ 低于”)理论产量。本实验所得到的环已烯质量为6.5g,则产率是______(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列排列顺序不正确的是( )
A.元素的非金属性:N<O<F
B.酸性:HClO4>H2SO4>H3PO4
C.热稳定性:HF>HCl>H2S
D.原子半径:Al>Mg>Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述中正确的是
A. 标准状况下,2.24 LCCl4中含有的氯原子数为0.4NA
B. 常温常压下,36g等体积混合的CO与CO2混合气体中含有的氧原子数为1.5NA
C. 1molFe与足量氯气反应时转移的电子数为2NA
D. 1L1mol·L-l的NaClO溶液中含有ClO-的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了抵御海水的侵蚀,往往会在船体上安装大型的锌块,利用原电池反应:2Zn+2H2O+O2 = 2Zn(OH)2,下列说法正确的是
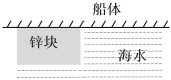
A. 锌块作为原电池的负极,发生还原反应而被腐蚀
B. 海水中的电解质如NaCl起到了导电的作用
C. 正极的电极反应式为:Zn - 2e-=Zn2+
D. 实际应用中,需用锌块覆满船体,完全隔绝海水以防止钢铁被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酯的合成路线如下图所示
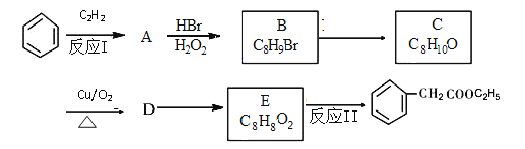
(1)反应Ⅰ反应类型为___________________; D中含氧官能团为_____________写名称)。
(2)反应Ⅱ的反应条件为:_________________。
(3)C→D的化学反应方程式为________________________________________。
(4)写出一种满足下列条件的E的同分异构体的结构简式为__________________________。
①能发生银镜反应 ②含苯环且苯环上一溴代物两种 ③不能与钠反应
(5)写出B合成![]() 的合成路线。合成路线常用的表示方式为:_______________
的合成路线。合成路线常用的表示方式为:_______________
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com