
| A、溶液呈电中性,胶体带有电荷 |
| B、Fe(OH)3胶体粒子在电场影响下将向阳极运动 |
| C、溶液中通过光束没有特殊现象,胶体中通过光束有丁达尔现象 |
| D、通电后,溶液中溶质粒子一定分别向两极移动,而胶体中分散质粒子向某一极移动 |


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
| A、原子的核外电子层数等于该元素所在周期数 |
| B、元素周期表中从ⅢB族到ⅡB族10列的元素都是金属元素 |
| C、稀有气体元素原子的最外层电子数都是8个 |
| D、主族元素原子最外层电子数等于族序数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能使酸性高锰酸钾溶液褪色 |
| B、能在空气中燃烧 |
| C、能使溴水褪色 |
| D、与HCl在一定条件下能加成只得到一种产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、NH4+、Cl-、SO42- |
| B、Na+、K+、HCO3-、NO3- |
| C、Na+、Cu2+、Cl-、NO3- |
| D、Mg2+、Na+、H2PO4-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.15 mol?(L?s)-1 |
| B、v(B)=0.6 mol?(L?s)-1 |
| C、v(C)=0.4 mol?(L?s)-1 |
| D、v(D)=0.45 mol?(L?s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:3:3 |
| B、3:1:2 |
| C、3:2:3 |
| D、1:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
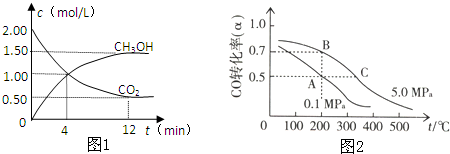
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com