

| 16×2 |
| 27.1% |
| 84 |
| 12 |
| 16×2 |
| 27.1% |
| 84 |
| 12 |
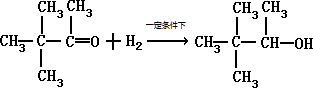 ,故答案为:
,故答案为: .
.


 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 | - |
| C6H5OH(苯粉) | C5H5OH?C6H5O-+H+ | 1.1×10-10 | |
| NH3?H2O | NH3?H2O?NH4++OH- | 1.76×10-5 | - |
| BaSO4 | BaSO4(s)?Ba2++SO42-(aq) | - | 1.07×10-10 |
| BaCO3 | BaCO3(s)?Ba2++CO32-(aq) | - | 2.58×10-9 |

查看答案和解析>>
科目:高中化学 来源: 题型:
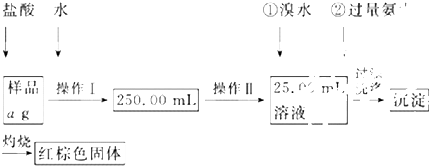
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、几种物质都有 |
| B、有甲酸乙酯和甲酸 |
| C、有甲酸乙酯和甲醇 |
| D、有甲酸乙酯,可能有甲醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有A、B、C、D、E、F6种有机物,它们是烃或者烃的衍生物,在一定的条件下可以有如图的转化关系:
有A、B、C、D、E、F6种有机物,它们是烃或者烃的衍生物,在一定的条件下可以有如图的转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com