
【题目】下列图示与对应的叙述相符的是
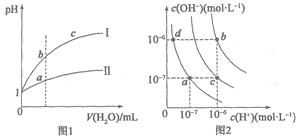
A.图1表示相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线II为盐酸,且b点溶液的导电性比a点强
B.图1中,中和等体积的两种酸,消耗等浓度的NaOH溶液体积V(I)>V(II)
C.图2中纯水仅升高温度,就可以从a点变到c点
D.图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
【答案】D
【解析】
在图Ⅰ中,盐酸与醋酸的pH相同,加水稀释相同的倍数后,盐酸溶液的pH变化大,所以Ⅰ为盐酸,Ⅱ为醋酸。
A.相同pH的盐酸和醋酸分别加水稀释相同倍数时,盐酸的pH变化大,所以曲线Ⅰ应为盐酸,A错误;
B. 因为盐酸和醋酸的pH相同,所以醋酸溶液的浓度大,中和等体积的两种酸,消耗等浓度的NaOH溶液体积V(I)< V(II),B错误;
C. 图2中纯水仅升高温度,c(H+)、c(OH-)同等程度增大且相等,不可能从a点变到c点,C错误;
D. 图2中在b点对应温度下,KW=10-12,pH=2的H2SO4中,c(H+)=10-2mol/L;pH=10的NaOH溶液中,c(OH-)=10-2mol/L,二者等体积混合后,刚好完全反应,溶液呈中性,D正确。
故选D。


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】乙烯是合成纤维、合成橡胶、合成塑料、合成乙醇![]() 酒精
酒精![]() 的基本化工原料,也用于制造氯乙烯、苯乙烯、环氧乙烷、醋酸、乙醛、乙醇和炸药等。世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一。工业上常采用烷烃裂解的方法制备乙烯。回答下列问题:
的基本化工原料,也用于制造氯乙烯、苯乙烯、环氧乙烷、醋酸、乙醛、乙醇和炸药等。世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一。工业上常采用烷烃裂解的方法制备乙烯。回答下列问题:
![]() 已知
已知![]() 、
、![]() 、
、![]() 的燃烧热分别为
的燃烧热分别为![]() 、
、![]() 、
、![]() 。利用乙烷制备乙烯的化学方程式
。利用乙烷制备乙烯的化学方程式![]()
![]() 。
。
![]() ________
________![]() 。
。
![]() 一定温度下,将
一定温度下,将![]() 加入固定体积的密闭容器中发生上述反应,下列能够表示到达平衡状态有________
加入固定体积的密闭容器中发生上述反应,下列能够表示到达平衡状态有________![]() 填字母
填字母![]() 。
。
A ![]()
![]() 气体压强不再变化
气体压强不再变化
C 气体的密度不再变化 D ![]() 的体积分数不再变化
的体积分数不再变化
![]() 在某密闭容器中通入
在某密闭容器中通入![]() ,正丁烷
,正丁烷![]() ,在不同条件下发生反应
,在不同条件下发生反应![]() ,正丁烷
,正丁烷![]() ,测得平衡时
,测得平衡时![]() 的体积分数
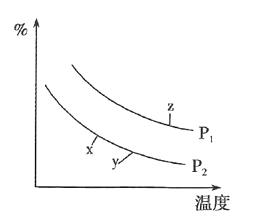
的体积分数![]() 与温度、压强的关系如图所示。
与温度、压强的关系如图所示。
![]() ________
________![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ,欲提高乙烯的产率,下列措施可行的是________。
,欲提高乙烯的产率,下列措施可行的是________。
A 加压升温 ![]() 加压降温
加压降温
C 减压降温 ![]() 减压升温
减压升温
E.选择优质催化剂
![]() 、y、z三点的化学平衡常数大小关系为________。
、y、z三点的化学平衡常数大小关系为________。
![]() 若z点对应的纵坐标的数值为50,此时
若z点对应的纵坐标的数值为50,此时![]() 的转化率为________,该条件下的化学平衡常数
的转化率为________,该条件下的化学平衡常数![]() ________
________![]() 用含有
用含有![]() 的表达式表示,
的表达式表示,![]() 为以分压表示的平衡常数
为以分压表示的平衡常数![]() 。
。
![]() 最近,中科院研究将甲烷在催化作用下脱氢后发生偶联反应生成乙烯,反应原理为:
最近,中科院研究将甲烷在催化作用下脱氢后发生偶联反应生成乙烯,反应原理为:![]() ,反应同时存在副反应:
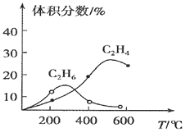
,反应同时存在副反应:![]() ,实验测得产物的体积分数受温度影响变化如图所示,制取乙烯应控制的反应温度为________
,实验测得产物的体积分数受温度影响变化如图所示,制取乙烯应控制的反应温度为________![]() ,温度过高,乙烯的体积分数反而减少的主要原因是________。
,温度过高,乙烯的体积分数反而减少的主要原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为84。回答下列问题:
(1)物质的量相同,下列物质充分燃烧与A消耗氧气的量不相等的是(填序号)__。
A.C7H12O2 B.C6H14 C.C6H14O D.C7H14O3
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为___。
(3)若A的名称为2-乙基-1-丁烯,核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为___。
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】姜黄素是一种天然染料,工业上可用石油的裂解产物通过如图反应制得:
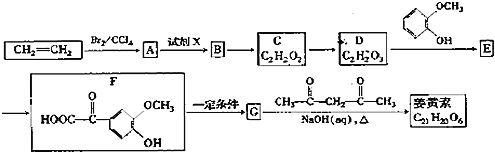
已知:![]()
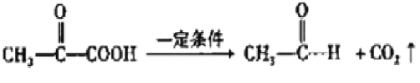
![]() CH3CHO+
CH3CHO+![]()
![]()
![]() +H2O
+H2O
请回答下列问题:
![]() 试剂X为 ______ ;
试剂X为 ______ ;
![]() 最多能消耗Na、NaOH、
最多能消耗Na、NaOH、![]() 的物质的量分别为3mo1、2mol、1mol,则E的结构简式为 ______ ;
的物质的量分别为3mo1、2mol、1mol,则E的结构简式为 ______ ;
![]() 姜黄素中的含氧官能团除甲氧基
姜黄素中的含氧官能团除甲氧基![]() 外还有 ______
外还有 ______ ![]() 写名称
写名称![]() ;
;
![]() 反应
反应![]() 的化学方程式为 ______ ,其反应类型是 ______ ;
的化学方程式为 ______ ,其反应类型是 ______ ;
![]() 符合下列条件G的同分异构体共有 ______ 种,其中核磁共振氢谱中有5组峰,且面积比为2:2:2:1:1的是 ______ ;
符合下列条件G的同分异构体共有 ______ 种,其中核磁共振氢谱中有5组峰,且面积比为2:2:2:1:1的是 ______ ;
①属于芳香酯类 ②苯环上有两个取代基 ③能与![]() 溶液发生显色反应
溶液发生显色反应
![]() 借鉴制取姜黄素的方法也能合成肉桂醛(
借鉴制取姜黄素的方法也能合成肉桂醛(![]() ),写出制备肉桂醛所需有机物的结构简式 ______ 。
),写出制备肉桂醛所需有机物的结构简式 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.1000mol·L-1的NaOH溶液分别滴定20.00mL均为0.1000mol·L-1的三种酸HX、HY、HZ ,滴定曲线如图所示。下列说法错误的是
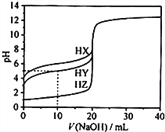
A. HZ是强酸,HX、HY是弱酸
B. 根据滴定曲线,可得Ka(HY)≈10-5
C. 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D. 将上述HY与HZ溶液等体积混合达到平衡时:C(H+)=c(OH-)+c(Z-)+c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(有机化学基础选做题)下列关系正确的是
A.沸点:乙二醇>丙三醇
B.与钠反应的快慢:CH3CH2COOH>苯酚>水>乙醇
C.等质量的有机物完全燃烧的耗氧量:甲烷>乙烯>乙炔>苯
D.同物质的量的物质燃烧耗O2量:己烷>环己烷>苯>苯甲酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍能形成多种不同的化合物。图1是镍的一种配合物的结构,图2是一种镍的氧化物的晶胞。判断下列说法正确的是

A.图2可能表示的是NiO的晶胞
B.图1中C、N、O的第一电离能C>N>O
C.图2中离镍原子最近的镍原子数共为8个
D.图1分子中存在的化学键有共价键、配位键、氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳族元素的单质及其化合物是一类重要物质。请回答下列问题:
(1)锗(Ge)是用途很广的半导体材料,基态Ge原子的核外电子中,有_____个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是________________________________________。
(3)GeCl4可水解生成一种氧化物和一种无氧酸,其化学反应方程式为:_______________。
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是____________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为______,微粒之间存在的作用力是_______。
(6)合成氮化碳是一种硬度比金刚石还大的晶体,氮化碳的晶体类型为________,该晶体中微粒间的作用力是____________。
(7)COCl2俗称光气,分子中C原子采取sp2杂化成键,光气分子的结构式为____________,其中碳氧原子之间共价键是________(填序号)。
a.2个σ键b.2个π键c.1个σ键,1个π键
(8) CaC2中C22与O22+互为等电子体,O22+的电子式可表示为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cu和浓硫酸反应(装置中的夹持、加热仪器省略),反应后,圆底烧瓶内的混合液倒入水中,得到蓝色溶液与少量黑色不溶物。
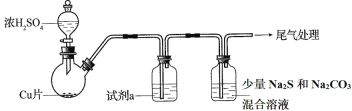
(1)反应后蓝色溶液呈酸性的原因有①______________,②______________。
(2)为检验反应产生气体的还原性,试剂 a 是______________。
(3)已知酸性:H2SO3>H2CO3>H2S。反应后测得 Na2S 和 Na2CO3 混合溶液中有新气体生成。该气体中 ______________ (填“含或不含”) H2S,理由是______________;
(4)少量黑色不溶物不可能是 CuO 的理由是______________。
查阅资料后发现该黑色固体可能是 CuS 或 Cu2S 中的一种或两种,且 CuS 和 Cu2S 在空气中煅烧易转 化成 Cu2O 和 SO2。称取 2.000g 黑色固体,灼烧、冷却、……最后称得固体 1.680g。
(5) 灼烧该固体除用到酒精灯、坩埚、坩埚钳、三脚架等仪器,还需要______________。 确定黑色固体灼烧充分的依据是______________,黑色不溶物其成分化学式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com