
【题目】常温下向10mL ![]() 的HR溶液中逐滴滴入
的HR溶液中逐滴滴入![]() 的
的![]() 溶液,所得溶液pH及导电性变化如下图。下列分析不正确的是
溶液,所得溶液pH及导电性变化如下图。下列分析不正确的是![]()
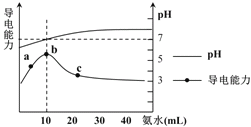
A.![]() 点导电能力增强说明HR为弱酸
点导电能力增强说明HR为弱酸
B.b点溶液![]() 说明
说明![]() 没有水解
没有水解
C.c 点溶液存在![]() 、
、![]()
D.![]() 任意点溶液均有
任意点溶液均有![]()
![]()
【答案】B
【解析】
A.溶液导电能力与离子浓度成正比,如果HR是强电解质,加入氨水至溶液呈中性时,溶液中离子浓度会减小,导致溶液导电能力降低,根据图知,加入氨水至溶液呈中性时随着氨水的加入,溶液导电能力增强,说明离子浓度增大,则HR为弱电解质,故A正确;
B.弱离子在水溶液中会发生水解反应,根据A知,HR是弱电解质,且一水合氨是弱电解质,所以![]() 是弱酸弱碱盐,b点溶液呈中性,且此时二者的浓度、体积都相等,说明HR和一水合氨的电离程度相等,所以该点溶液中铵根离子和酸根离子水解程度相等,故B错误;
是弱酸弱碱盐,b点溶液呈中性,且此时二者的浓度、体积都相等,说明HR和一水合氨的电离程度相等,所以该点溶液中铵根离子和酸根离子水解程度相等,故B错误;
C.c点溶液的![]() ,说明溶液呈碱性,溶液中
,说明溶液呈碱性,溶液中![]() ,再结合电荷守恒得
,再结合电荷守恒得![]() ,故C正确;
,故C正确;
D.离子积常数只与温度有关,温度不变,离子积常数不变,所以![]() 任意点溶液均有
任意点溶液均有![]()
![]() ,故D正确;
,故D正确;
故选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)乙同学认为甲同学的结论是错误的,他的理由是__________________________(用化学方程式表示),所以他认为应该检验__________(填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。
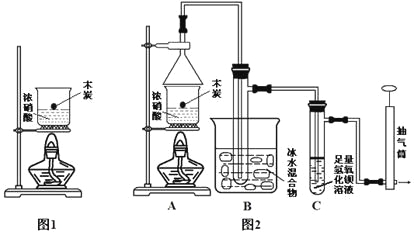
(2)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号)_______。
①将炭与浓硝酸一同放在装置中加热;②先加热浓硝酸,然后将炭投入其中;
③先加热炭,再加入冷浓硝酸; ④先加热炭,再将炭投入冷浓硝酸。
(3)请用平衡移动原理解释B装置的作用____________________________________。
(4)C装置中出现的现象是_______________________________________________,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的化学方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
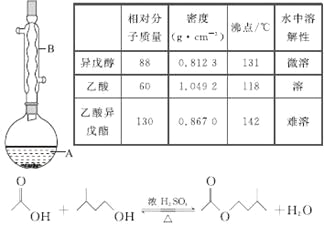
实验步骤:
在A中加入4.4 g异戊醇、6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50 min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的名称是________________。
(2)在洗涤操作中,第一次水洗的主要目的是_______________,第二次水洗的主要目的是________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是_______________________。
(5)实验中加入少量无水MgSO4的目的是________。
(6)在蒸馏操作中,仪器选择及安装都正确的是________(填标号)。
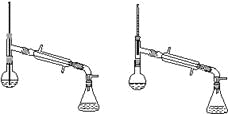
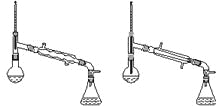
a. b. c. D.
(7)本实验的产率是________(填标号)。
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130 ℃便开始收集馏分,会使实验的产率偏__________(填“高”或“低”),其原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量A、B混合气体发生反应:aA(g)+bB(g) ![]() cC(g)。平衡时测得A的浓度为0.5 mol/L;保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度为0.28 mol/L。下列有关判断不正确的是( )
cC(g)。平衡时测得A的浓度为0.5 mol/L;保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度为0.28 mol/L。下列有关判断不正确的是( )
A.a+b>cB.C的体积分数增大
C.该变化使平衡逆向移动D.B的转化率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2molL-1。下列判断错误的是
xC(g)+2D(g)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2molL-1。下列判断错误的是
A. x=1B. 若混合气体的密度不变则表明该反应达到平衡状态
C. B的转化率为40%D. 2min内A的反应速率为0.3molL-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某酸HA的电离常数:K=1×10-5,下列说法正确的是
A. HA溶液中加入NaA固体后,![]() 减小
减小
B. 常温下,0.1mol/LHA溶液中水电离的c(H+)为10-13mol/L
C. NaA溶液中加入HCl溶液至恰好完全反应,存在关系:2c(Na+)=c(A-)+ c(Cl-)
D. 常温下,0.1mol/LNaA溶液水解常数为10-9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

①该反应的化学方程式为____________________________。
②从开始至2min,Z的平均反应速率为________________。
③若要提高X的转化率,请提出两条合理措施_______________________________、____________________________。
II.某探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如表所示:
实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气 所需时间/s |
Ⅰ | 薄片 | 15 | 200 |
Ⅱ | 薄片 | 25 | 90 |
Ⅲ | 粉末 | 25 | 10 |
①该实验的目的是探究__________、__________对锌和稀盐酸反应速率的影响;
②实验Ⅰ和Ⅱ表明__________,化学反应速率越大;
③能表明固体的表面积对反应速率有影响的实验编号是 ______ 和 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组同学对不同条件下铁钉的锈蚀进行了实验。
实验序号 | ① | ② | ③ | ④ |
实验 内容 |
|
|
|
|
一周后观察:
(1)铁钉被腐蚀程度最大的是___(填实验序号)。
(2)实验③中主要发生的是____(填“化学腐蚀”或“电化学腐蚀”)。
(3)烧过菜的铁锅未及时洗净(含氯化钠的残留液),第二天便出现红棕色锈斑,试写出有关的电极反应式: 负极____;
(4)根据上述实验,你认为铁发生电化学腐蚀的条件是____。
(5)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有___(填序号)。
①健身器材刷油漆 ②自行车钢圈镀铬 ③将钢管用导线与镁条连接 ④将钢管用导线与碳棒连接
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 恒容密闭容器中进行的反应:A(s)+3B(g)![]() 2C(g)+D(g),如果气体密度保持不变,说明反应已经达到平衡
2C(g)+D(g),如果气体密度保持不变,说明反应已经达到平衡
B. C ( s) + H2O (g) ![]() CO ( g) + H2 (g),其他条件不变,缩小容器体积,正速率减小,逆速率增大
CO ( g) + H2 (g),其他条件不变,缩小容器体积,正速率减小,逆速率增大
C. N2(g) + 3H2(g)![]() 2NH3(g) △H=—93kJ·mol—1,往恒容密闭容器中充入0.4 molN2(g)和2 mol H2(g)达到平衡时,可以放出37.2 kJ的热量
2NH3(g) △H=—93kJ·mol—1,往恒容密闭容器中充入0.4 molN2(g)和2 mol H2(g)达到平衡时,可以放出37.2 kJ的热量
D. A(g)+ 3B (g) ![]() 2C (g) + D (g),在两种不同情况下的反应速率分别为:①
2C (g) + D (g),在两种不同情况下的反应速率分别为:①![]() ,②
,②![]() ,则前者比后者快
,则前者比后者快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com