
����Ŀ����Ҫ��ش���������:
(1)�ڱ�״���£�CO��CO2������������Ϊ32g,���Ϊ22.4L��������CO��CO2���ʵ���֮��Ϊ_____________������Oԭ�ӵ���ĿΪ_____________�������е�CO2�������Ĺ������Ʒ�Ӧ����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ_____________��
(2)��ʵ���ҽ�16.8g����NaHCO3����һ��ʱ����ʣ������������Ϊ13.7g������ٵ�Ϊ_______���ʵ���������______gNaHCO3�����˷ֽⷴӦ��
���𰸡� 3:1 1.25��6.02��1023 0.25mol CO2��H2O 8.4
��������(1)��״���£�CO��CO2������������Ϊ32g�����Ϊ22.4L�������������ʵ�����1mol���������ƽ����Է���������32������ʮ�ֽ��淨��֪CO��CO2���ʵ���֮��Ϊ![]() ������CO��CO2�����ʵ����ֱ���0.75mol��0.25mol���������Oԭ�ӵ����ʵ�����1.25mol����ĿΪ1.25��6.02��1023��0.25molCO2�������Ĺ������Ʒ�Ӧ����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ0.25mol��(2)��Ӧ���������������16.8g��13.7g��3.1g�����ݷ���ʽ��֪
������CO��CO2�����ʵ����ֱ���0.75mol��0.25mol���������Oԭ�ӵ����ʵ�����1.25mol����ĿΪ1.25��6.02��1023��0.25molCO2�������Ĺ������Ʒ�Ӧ����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ0.25mol��(2)��Ӧ���������������16.8g��13.7g��3.1g�����ݷ���ʽ��֪
2NaHCO3![]() Na2CO3��H2O��CO2�� ������������
Na2CO3��H2O��CO2�� ������������
168 106 18 44 62
8.4g 3.1g
���Լ��ٵ�ΪCO2��H2O����������8.4gNaHCO3�����˷ֽⷴӦ��


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����14gͭ���Ͻ���������HNO3��Ӧ���ų����������״�������Ϊ1.12L��O2 ��Ϻ���ͨ��ˮ�У�ǡ��ȫ�����գ���Ͻ���ͭ������Ϊ
A. 4.8g B. 3.2g C. 6.4g D. 10.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ù��������MMF����������ֲ������ϸ����ֳ��õ�ҩ�����˵����ȷ���ǣ� �� 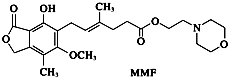
A.MMF������ˮ
B.1 mol MMF���뺬3 mol NaOH��ˮ��Һ��ȫ��Ӧ
C.1 mol MMF����6 mol���������ӳɷ�Ӧ
D.MMF�ܷ���ȡ����Ӧ����ȥ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС���������������������װ�ã���ͼ1�����Ի������Ʊ�����ϩ��
��֪�� ![]()
�ܶȣ�g/cm3�� | �۵㣨�棩 | �е㣨�棩 | �ܽ��� | |
������ | 0.96 | 25 | 161 | ������ˮ |
����ϩ | 0.81 | ��103 | 83 | ������ˮ |
��1���Ʊ���Ʒ��12.5mL�����������Թ�A�У��ټ���1mLŨ���ᣬҡ�Ⱥ�������Ƭ��������������Ӧ��ȫ�����Թ�C�ڵõ�����ϩ��Ʒ��
��A�����Ƭ�������� �� ����B���˵�������е������� ��
���Թ�C���ڱ�ˮԡ�е�Ŀ���� ��
��2���Ʊ���Ʒ�ٻ���ϩ��Ʒ�к��л������������������ʵȣ����뱥��ʳ��ˮ�������á��ֲ㣬����ϩ���㣨��ϡ����¡�������Һ��������ѡ����ĸ��ϴ�ӣ�
a��KMnO4��Һ b��ϡ���� c��Na2CO3��Һ
���ٽ�����ϩ����ͼ2װ��������ȴˮ�����룮����ʱҪ������ʯ�ң�Ŀ���� ��
���ռ���Ʒʱ�����Ƶ��¶�Ӧ�����ң�ʵ���ƵõĻ���ϩ��Ʒ�����������۲��������ܵ�ԭ��������ѡ����ĸ����
a������ʱ��70�濪ʼ�ռ���Ʒ
b��������ʵ����������
c���Ʊ���Ʒʱ���������Ʒһ������
��3���������ֻ���ϩ��Ʒ�ʹ�Ʒ�ķ�����������������ѡ����ĸ����a�������Ը��������Һ b���ý����� c������ˮ d���ⶨ�е㣮
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������᳧����(�����������������FeS��SiO2)�Ƽ�ʽ����������������:

(1)SO2�����NaOH��Һ��Ӧ�����ӷ���ʽΪ_____________��
(2)��������Ҫ�ɷ�Ϊ_________(�ѧʽ)��
(3)��Ӧ1�м�˫��ˮ��Ŀ���ǽ�Fe2+����ΪFe3+,�÷�Ӧ�����ӷ���ʽΪ________��
(4)��ʽ�������Ļ�ѧʽΪFex(OH)y(SO4)z��nH2O��Ϊȷ������ɽ�������ʵ�飺
�ٳ�ȡ1.6920g��Ʒ����������ϡ�����У�
�ڼ�������BaCl2��Һ�����ˡ�ϴ�ӡ�������أ��ù�������Ϊ2.3300g��
������ڵ���Һ�мӹ�����NaOH��Һ�����ˡ�ϴ�ӡ����ա����أ��ù�������Ϊ0.6400g��
��������ʵ������ȷ���ü�ʽ�������Ļ�ѧʽ_________(д���������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A. 2g��������ԭ����ĿΪ1mol
B. 1molO2��������32g
C. �����Ħ��������98g
D. ����Ħ����������ֵ�ϵ�����ԭ�ӵ����ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�H2��g��+CO2��g��H2O��g��+CO��g����ƽ�ⳣ��K= ![]() �����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2��g����CO2��g��������ʼŨ�������ʾ�������жϲ���ȷ���ǣ� ��
�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2��g����CO2��g��������ʼŨ�������ʾ�������жϲ���ȷ���ǣ� ��
��ʼŨ�� | �� | �� | �� |
c��H2��/mol/L | 0.010 | 0.020 | 0.020 |
c��CO2��/mol/L | 0.010 | 0.010 | 0.020 |
A.ƽ��ʱ������CO2��ת���ʴ���60%
B.ƽ��ʱ�����кͱ���H2��ת���ʾ���60%
C.ƽ��ʱ������c��CO2���Ǽ��е�2������0.012mol/L
D.��Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�����ȷ���ǣ� ��
A. 14N��15N������ͬ�������� B. 18O��17O������ͬ�ĵ�����
C. 18O��19F������ͬ�������� D. 12C��13C������ͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������кͷ�Ӧ�ı����ǣ�H+ + OH�� = H2O���������ʼ�ķ�Ӧ�������������ӷ���ʽ��ʾ����( )
A. ����������ϡ���ᷴӦ B. Ba(OH)2��Һ����ϡ������
C. ����ʯ��ˮ��ϡ���ᷴӦ D. ��ˮ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com