
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示:
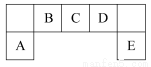
(1)B、C、D元素电负性的大小顺序为: > > (填元素符号)。
(2)E的氢化物与其最高价氧化物对应的水化物的钾盐共热能发生反应生成一种气体单质,反应的化学方程式为 。
(3)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L甲气体与0.5 L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是 。
(4)在298 K下,A、B的单质各1 mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3 mol B的单质,则该反应在298 K下的ΔH= 。(注:题中所设单质均为最稳定单质)
(5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是 。
(6)用A、B的单质作电极,C的最高价氧化物对应水化物的浓溶液作电解质溶液构成原电池,写出此原电池正极的电极反应式 。(假设C只被还原至+4价)
(1)O;N;C (2)8HCl+KClO4 KCl+4Cl2↑+4H2O (3)NaNO2 (4)-(4a-3b) kJ/mol或(3b-4a) kJ/mol (5)将氯水(或氯气)滴入(或通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成(答案合理即可) (6)NO3-+e-+2H+=NO2↑+H2O
KCl+4Cl2↑+4H2O (3)NaNO2 (4)-(4a-3b) kJ/mol或(3b-4a) kJ/mol (5)将氯水(或氯气)滴入(或通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成(答案合理即可) (6)NO3-+e-+2H+=NO2↑+H2O
【解析】由已知的元素周期表的结构可推知:A、B、C、D、E五种元素分别是Al、C、N、O、Cl。(1)电负性O>N>C。(2)生成的气体单质是Cl2,反应的化学方程式为:8HCl+KClO4 KCl+4Cl2↑+4H2O。(3)氮的氧化物中,NO的相对分子质量最小,2 L NO与0.5 L O2混合后先生成1 L NO与1 L NO2的混合气体,再与NaOH溶液发生下列反应:NO+NO2+2NaOH=2NaNO2+H2O,所以生成的盐是NaNO2(也可用电子守恒法推出N在盐中显+3价,所以是NaNO2)。(4)在298 K下,1 mol Al(s)完全燃烧放出热量a kJ,1 mol C(s)完全燃烧放出热量b kJ,根据盖斯定律可得,该反应在298 K下的ΔH为-(4a-3b) kJ·mol-1或(3b-4a) kJ·mol-1。(5)要证明S的非金属性与Cl的非金属性强弱,可以利用置换反应,将氯水(或氯气)滴入(或通入)硫化钠(或硫化氢等)溶液中即可(答案合理即可)。(6)常温下,Al被浓硝酸钝化,碳与浓硝酸反应生成CO2和NO2,故碳为原电池负极,正极上硝酸得电子生成NO2。
KCl+4Cl2↑+4H2O。(3)氮的氧化物中,NO的相对分子质量最小,2 L NO与0.5 L O2混合后先生成1 L NO与1 L NO2的混合气体,再与NaOH溶液发生下列反应:NO+NO2+2NaOH=2NaNO2+H2O,所以生成的盐是NaNO2(也可用电子守恒法推出N在盐中显+3价,所以是NaNO2)。(4)在298 K下,1 mol Al(s)完全燃烧放出热量a kJ,1 mol C(s)完全燃烧放出热量b kJ,根据盖斯定律可得,该反应在298 K下的ΔH为-(4a-3b) kJ·mol-1或(3b-4a) kJ·mol-1。(5)要证明S的非金属性与Cl的非金属性强弱,可以利用置换反应,将氯水(或氯气)滴入(或通入)硫化钠(或硫化氢等)溶液中即可(答案合理即可)。(6)常温下,Al被浓硝酸钝化,碳与浓硝酸反应生成CO2和NO2,故碳为原电池负极,正极上硝酸得电子生成NO2。


科目:高中化学 来源:2014年高考化学苏教版总复习 7-2 化学反应的方向和限度练习卷(解析版) 题型:选择题
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1。
2NH3(g) ΔH=-92.4 kJ·mol-1。
实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量a kJ |
② | 2 | 3 | 0 | 放出热量b kJ |
③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是( )
A.放出热量关系:a<b<92.4
B.三个容器内反应的平衡常数:③>①>②
C.达平衡时氨气的体积分数:①>③
D.N2的转化率:②>①>③
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 6-2 原电池、常见的化学电源练习卷(解析版) 题型:填空题
根据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示,其中盐桥为琼胶?饱和KNO3盐桥。请回答下列问题。( )
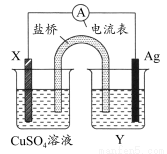
(1)电极X的材料是________,电解质溶液Y是________。
(2)银电极为电池的________极,写出两电极的电极反应式:
银电极:_________________________________________________;
X电极:___________________________________________________。
(3)外电路中,电子是从________电极流向________电极。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 6-1 化学反应中的热效应练习卷(解析版) 题型:填空题
(1)宇宙飞船上的氢氧燃料电池,其电池反应为:2H2+O2=2H2O,试写出电解质溶液若为盐酸时的正极反应式:______________。
(2)已知4 g甲烷气体充分燃烧生成CO2(g)和H2O(l)时,放出Q kJ的热量。写出表示甲烷燃烧热的热化学方程式:______________________。
(3)已知下列热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-Q1 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH=-Q2 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=-Q3 kJ/mol
利用盖斯定律计算:FeO(s)+CO(g)=Fe(s)+CO2(g)的焓变ΔH=________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 6-1 化学反应中的热效应练习卷(解析版) 题型:选择题
参照反应Br+H2 HBr+H的能量对反应历程的示意图。下列叙述正确的是( )
HBr+H的能量对反应历程的示意图。下列叙述正确的是( )
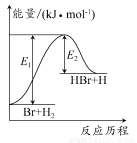
A.正反应为放热反应
B.加入催化剂,该化学反应的反应热变大
C.反应物总能量低于生成物总能量
D.升高温度可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 5-2 元素周期律 元素周期表练习卷(解析版) 题型:选择题
下表是元素周期表的一部分,有关说法正确的是( )
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 |
|
|
| c |
| d |
|
3 | a | b |
|
|
| e | f |
A.e的氢化物比d的氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.六种元素中,c元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 5-2 元素周期律 元素周期表练习卷(解析版) 题型:选择题
短周期元素X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍,下列说法正确的是( )
A.X的最高价氧化物对应的水化物显弱酸性
B.Y的氧化物是离子化合物
C.X的氢化物的水溶液在空气中存放不易变质
D.X的氢化物和Z的氢化物反应生成一种对热稳定的化合物
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 5-1 人类对原子结构的认识练习卷(解析版) 题型:选择题
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子。在ag HmX中所含质子的物质的量是( )
A. (A-N+m) mol B.
(A-N+m) mol B.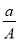 (A-N) mol
(A-N) mol
C.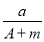 (A-N) mol D.
(A-N) mol D.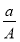 (A-N+m) mol
(A-N+m) mol
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 3-1 从铝土矿到铝合金练习卷(解析版) 题型:选择题
某溶液中可能含有大量的Mg2+、Al3+、H+、Cl-和少量OH-,向该溶液中逐滴加入0.5 mol·L-1的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如图所示,则该溶液中( )
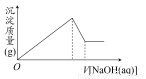
A.有Mg2+,没有Al3+
B.有Al3+,没有Mg2+
C.有大量的H+、Mg2+和Al3+
D.有Mg2+和Al3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com