
| X | |
| Y | Z |
科目:高中化学 来源:不详 题型:单选题
| A.H35Cl、H37Cl属于同素异形体 |
| B.16O与18O的中子数不同,核外电子排布却相同 |
| C.稳定性:CH4>SiH4;还原性:HCl>H2S |
| D.K+、Ca2+、Mg2+的离子半径依次增大,还原性依次增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | | 450 |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 元素主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
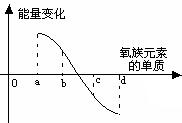
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.常温下,Z单质为气态物质 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物的稳定性要比X的氢化物的稳定性强 |
| D.Y元素的非金属性比W元素的非金属性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
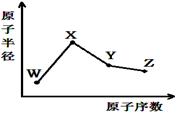
| A.对应气态氢化物的稳定性:Y>Z |
| B.化合物XZW既含离子键也含共价键 |
| C.对应简单离子半径:W>X |
| D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
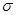 键和
键和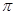 键数目之比为________,B、C、E三种元素的第一电离能由大到小的顺序为_________(用实际元素符号表示)。
键数目之比为________,B、C、E三种元素的第一电离能由大到小的顺序为_________(用实际元素符号表示)。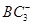 离子中B原子轨道的杂化类型为__________。
离子中B原子轨道的杂化类型为__________。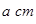 。该晶体的密度为________
。该晶体的密度为________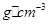 g(NA表示阿伏加德罗常数,E的相对原子质量为b)。
g(NA表示阿伏加德罗常数,E的相对原子质量为b)。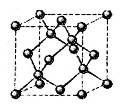
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.L、M、X三元素位于同一族 |
| B.K、Z两元素的氢化物的水溶液都显酸性 |
| C.Y元素对应的氢化物比K元素对应的氢化物沸点低 |
| D.K、L、X、Z四种元素离子半径大小顺序是Z->L+>X3+>K3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com