
����Ŀ����ʮ��������ѧ�����߶�̼�����������˹㷺������о���ȡ����һЩ��Ҫ�ɹ���������CO2��CH4�������ƺϳ�������Ҫ�ɷ�ΪCO��H2������֪���������в��ַ�Ӧ���Ȼ�ѧ����ʽΪ��
I��CH4��g���TC��s��+2H2��g����H=+75.0kJmol��1
II��CO2��g��+H2��g���TCO��g��+H2O��g����H=+41.0kJmol��1
III��CO��g��+H2��g���TC��s��+H2O��g����H=��131.0kJmol��1
��1����ӦCO2��g��+CH4��g���T2CO��g��+2H2��g���ġ�H=kJmol��1 ��
��2���̶�n��CO2��=n��CH4�����ı䷴Ӧ�¶ȣ�CO2��CH4��ƽ��ת���ʼ�ͼ�ף� 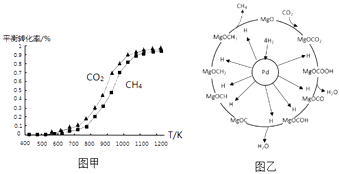
��ͬ�¶���CO2��ƽ��ת����������ڡ���С�ڡ���CH4��ƽ��ת���ʣ���ԭ����
�ڸ����½��и÷�Ӧʱ������ӦI���ɡ���̼����̼���ʣ�����ɴ����ж��������·�ӦI���Է����е�ԭ���� ��
��3��һ��������Pd��Mg/SiO2������ʹCO2�����黯���Ӷ����Ϊ�����䷴Ӧ������ͼ����ʾ���÷�Ӧ�Ļ�ѧ����ʽΪ
��4��CO�����ڹ�ҵұ����������ͼ���ڲ�ͬ�¶���CO��ԭ���ֽ����������ƽ���������lg[c��CO��/c��CO2��]���¶ȣ�t���Ĺ�ϵ����ͼ������˵����ȷ����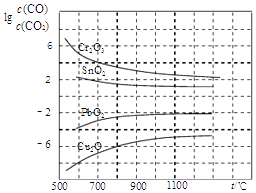
A.��ҵ�Ͽ���ͨ�����߷�Ӧװ�����ӳ���ʯ��
CO�Ӵ���ʱ�䣬����β����CO�ĺ���
B.CO���������ڹ�ҵұ����������Cr��
C.��ҵұ������ͭ��Cu��ʱ�ϵ͵��¶�������
���CO��������
D.CO��ԭPbO2�ķ�Ӧ��H��0
��5�������˺�������Ӧ�õ绯ѧԭ������PtΪ������Pb��CO2�����壩Ϊ������KHCO3��ҺΪ�������Һ����ԭ������������CO2ͬʱ����O2���µ���ԴCO���ܷ�Ӧ�Ļ�ѧ����ʽΪ��2CO2 ![]() 2CO+O2 �� ���������ĵ缫��ӦʽΪ ��
2CO+O2 �� ���������ĵ缫��ӦʽΪ ��
���𰸡�
��1��+247
��2�����ڣ�CO2��������������Ӧ����S��0
��3��CO2+4H2 ![]() CH4+2H2O
CH4+2H2O
��4��BC
��5��4OH����4e��=O2��+2H2O
���������⣺��1����֪����CH4��g���TC��s��+2H2��g����H=+75.0kJ/mol
��CO2��g��+H2��g���TCO��g��+H2O��g����H=+41.0kJ/mol
��CO��g��+H2��g���TC��s��+H2O��g����H=��131.0kJ/mol
���ݸ�˹���ɢ�+�ک��۵õ���ӦCO2��g��+CH4��g���T2CO��g��+2H2��g������H=+247kJ/mol��
���Դ��ǣ�+247����2���ٸ���ͼʾ���Կ�����CO2��������������Ӧ��ͬ�¶���CO2��ƽ��ת���ʴ���CH4��ƽ��ת���ʴ��ڣ�
���Դ��ǣ����ڣ�CO2��������������Ӧ��
�ڷ�Ӧ�Է����е��оݣ���H��T��S��0����Ӧ�١�S��0����H��0�������оݣ��õ���Ӧ�ڸ��������Է����У�
���Դ��ǣ���S��0����3������Ϣ��һ��������Pd��Mg/SiO2������ʹCO2�����黯��������д������ʽΪ��CO2+4H2 ![]() CH4+2H2O��
CH4+2H2O��
���Դ��ǣ�CO2+4H2 ![]() CH4+2H2O����4��A������¯�ĸ߶ȣ�����CO������ʯ�ĽӴ�������Ӱ��ƽ���ƶ���CO�������ʲ��䣬��A����
CH4+2H2O����4��A������¯�ĸ߶ȣ�����CO������ʯ�ĽӴ�������Ӱ��ƽ���ƶ���CO�������ʲ��䣬��A����
B����ͼ���֪��CO��ҵұ��������ʱ��lg[c��CO��/c��CO2��]һֱ�ܸߣ�˵��COת���ʺܵͣ��ʲ��ʺ�B��ȷ��
C����ͼ���֪�¶�Խ��lg[c��CO��/c��CO2��]ԽС����COת����Խ�ߣ���C��ȷ��
D����ͼ���֪CO��ԭPbO2���¶�Խ��lg[c��CO��/c��CO2��]Խ�ߣ�˵��COת����Խ�ͣ�ƽ�������ƶ����ʡ�H��0����D����
���Դ��ǣ�BC����5����PtΪ������Pb��CO2�����壩Ϊ������KHCO3��ҺΪ�������Һ����ԭ������������CO2ͬʱ����O2���µ���ԴCO���ܷ�Ӧ�Ļ�ѧ����ʽΪ��2CO2 ![]() 2CO+O2 �� ����Һ�е���������������ʧȥ���ӷ���������Ӧ�����������缫��ӦʽΪ��4OH����4e��=O2��+2H2O��
2CO+O2 �� ����Һ�е���������������ʧȥ���ӷ���������Ӧ�����������缫��ӦʽΪ��4OH����4e��=O2��+2H2O��
���Դ��ǣ�4OH����4e��=O2��+2H2O��
�����㾫����ͨ��������÷�Ӧ�Ⱥ��ʱ�ͻ�ѧƽ��״̬���ʼ������������ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȣ���ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч�������Խ����⣮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ�������м��ס����㡢��Լ����ɫ���ŵ㣬�۲������ĸ������ʵ�������г�װ��δ���������ж�����˵����ȷ����
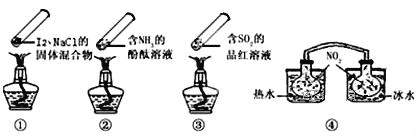
A. ����ʱ�����ϲ�����˹���⣬˵��������ȶ��Խϲ�
B. ����ʱ���������е���Һ����죬��ȴ���ֶ���Ϊ��ɫ
C. ���У���������ˮ�е�������������ɫ��������ڱ�ˮ�е�������������ɫ��dz
D. �ĸ������ʵ�����ж��п��淴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������ԭ��Ӧ�����Ƿ��ȷ�Ӧ���ǣ� ��
A.����ϡ����ķ�Ӧ
B.Ba��OH��28H2O��NH4Cl�ķ�Ӧ
C.���ȵ�̼�������̼�ķ�Ӧ
D.NaOH��HCl�ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ֧25mL����ʽ�ζ�����ʢ��0.1mol/L HCl��Һ����Һ��ǡ����5mL�Ŀ̶ȴ������ѵζ����е���Һȫ�������ձ��У�Ȼ����0.1mol/L NaOH��Һ���еζ���������NaOH��Һ������� ��
A.����20mL
B.��20mL
C.����20mL
D.����5mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���2mol A��2mol B���������������ݻ�Ϊ2L��ij�ܱ������У��������·�Ӧ3A��g��+B��g��xC��g��+2D��g����2minĩ��Ӧ�ﵽƽ��״̬��������0.8mol D�������C��Ũ��Ϊ0.4mol/L������д���пհף�
��1��xֵ���� ��
��2��A��ת����Ϊ ��
��3������D�ķ�Ӧ����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.��ѧ��Ӧ���ʱ��뷴Ӧ��;���й�
B.�����£�ϡ��0.1molL��1CH3COOH��Һ����Һ�ĵ�����������
C.���³�ѹ�£�22.4L Cl2�к��еķ�����Ϊ6.02��1023��
D.��������ͭ��a��b����;����ȫת��ΪCu��NO3��2 �� ;��a��b���ĵ�����һ����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���Ȼ�̼��һ����ɫ�ж��ӷ�Һ�壬������ˮ���ܶ�>1 g/cm3���е�ԼΪ76��8�档Ҫ��ˮ�����Ȼ�̼�Ļ�����ォ���Ȼ�̼������������з��������������
A. ���� B. ��Һ C. ���� D. ��ȡ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦA��g��+3B��g��2C��g��+2D��g����4�ֲ�ͬ����·�Ӧ���ʷֱ����£����з�Ӧ����v�����ǣ� ��
A.v��A��=9.0mol/��Lmin��
B.v��B��=0.6 mol/��Ls��
C.v��C��=0.3 mol/��Ls��
D.v��D��=0.1 mol/��Ls��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������H2�Ļ�ѧ��Ӧ��Zn + H2SO4 = ZnSO4 + H2�����÷�Ӧ�У���������_________,��������������_________������Ӧ����1 mol H2, ��Ӧ�е���ת�Ƶ����ʵ���Ϊ_________mol��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com