
����Ŀ����Ԫ�غ�̼Ԫ���γɵĵ��ʼ����������������������й㷺����;��
��ش��������⣺
��1����̬Feԭ�ӵļ۲���ӵĵ����Ų�ͼΪ_________________�����������ӵĵ�������״Ϊ___________��
��2��(NH4)2Fe(SO4)2 6H2O�׳�Ħ���Ρ��������ӵ�VSEPRģ������Ϊ____________________��
д��һ����NH4+��Ϊ�ȵ�����ķ��ӵĵ���ʽ��________________________________��
��3��Fe(CO)5���������������Ϳ�������.������ЦҼ��ͦм�����Ŀ֮��Ϊ______________��CO�ķе����N2��ԭ����_________________________��
��4��̼Ԫ�ؿ��γɶ��ֵ��ʡ�
��ʯīϩ�Ǵ�ʯī�а���������ɵ���̼ԭ�ӹ��ɵ�ƽ��ṹ����̼���ϡ�����̼ԭ�ӵ��ӻ���ʽΪ______________________��
�ϣ�����̼ԭ�ӵ��ӻ���ʽΪ ,
�ڽ��ʯ�ľ�����ͼ��ʾ������������Ϊa pm�������ӵ�������ֵΪNA����þ�����ԭ�ӵ����ռ��������İٷ���Ϊ________________��1cm3�����ƽ������Ϊ___________���г�����ʽ���ɣ���
���𰸡�  ���� ����������
���� ���������� 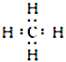 ����
����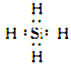 �� 1��1 ������Է���������ͬ��COΪ���Է��ӣ�N2Ϊ�Ǽ��Է��ӣ�CO�ķ��Ӽ�����������N2�� sp2 34%
�� 1��1 ������Է���������ͬ��COΪ���Է��ӣ�N2Ϊ�Ǽ��Է��ӣ�CO�ķ��Ӽ�����������N2�� sp2 34% ![]()
��������(1)��̬ F eԭ�ӵļ۲�����Ų�ʽΪ3d64s2���ɵ���۲���ӵĵ����Ų�ͼ�� ����������Ϊ 4s����,�ʵ�������״Ϊ���Ρ�
(2)SO42- �ļ۲���Ӷ���ĿΪ4,�� VSEPR ģ������Ϊ���������Ρ� ���ݵȵ�����ĺ�����ԭ��������ͬ�Ҽ۵������������ NH4 + ��Ϊ�ȵ�����ķ���ΪCH4 ��SiH4����д������ʽ��(3)Fe(CO)5������ Feԭ����5�� CO �γ�5���Ҽ���ÿ��CO �����к���1���Ҽ���2���м����ʶ��ߵ���
Ŀ֮��Ϊ1��1�� ������Է���������ͬ����ɺͽṹ����������Խǿ�����Ӽ�������Խ�����е�Խ����
(4)��ʯī��̼ԭ������������̼ԭ��֮���γ������Ҽ�,��ռ乹��Ϊƽ��������, ���ӻ� ��ʽΪsp2��
���ռ������ʵ��ھ�����ԭ��ʵ��ռ��������Ծ���������ɵ���ռ�������Ϊ34%��ÿ�����ʯ�ľ���ʵ��ռ��8��̼ԭ����������Ϊ��12��8��/ NA g�����������Ϊ( a��10-10)3cm3��1cm3 ������ƽ�����о�������ĿΪ1/(a��10-10)3,��1cm3 �����ƽ������Ϊ![]() ��
��


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������C2H4��NH3��Ƚϣ����н��۴������
A. ���ǵķ��Ӹ�����Ϊ17��28
B. ���ǵ�ԭ�Ӹ�����Ϊ17��28
C. ���ǵ���ԭ�Ӹ�����Ϊ17��21
D. ��������ͬ״���µ������17��21
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������H2��O2�Ʊ�H2O2��ԭ��Ϊ
�� H2(g)+ A(1)![]() B(1) ��H1 ��O2(g)+B(1)
B(1) ��H1 ��O2(g)+B(1)![]() A(1)+ H2O2(1) ��H2
A(1)+ H2O2(1) ��H2
��֪��A��B��Ϊ�л��������Ӧ�����Է����У�����˵����ȷ����
A. ��H2>0
B. BΪH2��O2�Ʊ�H2O2�Ĵ���
C. ��Ӧ�ٵ�����Ӧ�Ļ�ܴ����淴Ӧ�Ļ��
D. H2(g)+O2(g)![]() H2O2(1) �Ħ�H <0
H2O2(1) �Ħ�H <0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵����ȷ����
A. ������������������������֮��Ϊ1��1
B. �ױ��ܷ����ӳɷ�Ӧ��������Ӧ��ȡ����Ӧ
C. ����ϩ��ʹ����KMnO4��Һ����ˮ��ɫ��������ԭ����ͬ
D. ![]() ��C4H10�Ķ��ȴ������Ŀ��ͬ�����������칹��
��C4H10�Ķ��ȴ������Ŀ��ͬ�����������칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B������Ϊԭ�ϣ��ϳ����Ƹ�Ѫ֬ҩ��M��·��������ʾ�����ַ�Ӧ�������Լ���ȥ����


��֪����A���ܶ���ͬ������H2�ܶȵ�13����
��![]() ��R��ʾ��������
��R��ʾ��������
�� ��R1��R2��ʾ������
��R1��R2��ʾ������
��ش��������⣺
��1��B�Ļ�ѧ����Ϊ_______________��E�й����ŵĽṹʽΪ________________________��
��2��L�Ľṹ��ʽΪ_________________��M�ĺ˴Ź�����������___________�����շ塣
��3��A��C�ķ�Ӧ����Ϊ__________________________��
��4��I�ķ����������___________��̼ԭ����ͬһƽ���ϡ�
��5��J��K�Ļ�ѧ����ʽΪ________________________________________________��
��6���л���N��L������CH2���ţ�ͬʱ��������������N��ͬ���칹����___________�֣������������칹����
�ٱ�����������ȡ����
������FeCl3��Һ������ɫ��Ӧ
������NaHCO3��Һ��Ӧ����CO2
��7�����������ϳ�·�ߺ���Ϣ���� ���Ҵ�Ϊԭ�ϣ����Լ���ѡ��������Ʊ�2-�����������ĺϳ�·�ߣ�___________________________________________��
���Ҵ�Ϊԭ�ϣ����Լ���ѡ��������Ʊ�2-�����������ĺϳ�·�ߣ�___________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ʹ�ò��漰��ѧ�仯����
A. �������ׯ�ڡ� B. Һ�����������
C. ������γ� D. ��ʯ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״����VL�����ܽ���lLˮ��(ˮ���ܶȽ���Ϊ1g/mL)��������Һ���ܶ�Ϊ��g/mL�����������������ʵ���Ũ��Ϊcmol/L�����й�ϵ�в���ȷ����
A. ��=17c/(1000p) B. ��=17V/(17V+22400)
C. p=17V/(22.4+22.4V)/(17V+22400) D. c=1000Vp/(17V+22400)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaHCO3��Һ�м���Na2O2��������Ӧ�����ӷ���ʽ����Ϊ��________________________________, _____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���磭Fenton��������ˮ�����л���Ⱦ�オ��ĸ������������䷴Ӧԭ����ͼ��ʾ�����е�������H2O2��Fe2+����Fenton��Ӧ��H2O2+Fe2+=Fe3++OH������OH�����ɵ��ǻ����ɻ�(��OH)�����������л���Ⱦ�����˵������ȷ����
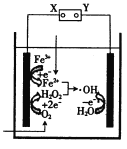
A����Դ��X��Ϊ������Y��Ϊ����
B�������ĵ缫��ӦʽΪFe2+��e��=Fe3+
C�������ĵ缫��ӦʽΪH2O��e��=H++��OH
D��ÿ����1molO2�����������������Ͽɲ���2mol��OH
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com