
【题目】Ⅰ. A、B、C、D、E均为中学化学常见的纯净物,B为最常见的液体,它们之间有如下反应关系:
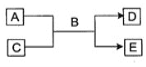
(1)若A为短周期的金属单质,D为气态单质,0.1 mol/L-1 C溶液的pH=13,则该反应的离子方程式为____________。
(2)若A的水溶液能使淀粉溶液变蓝,C为非金属氧化物,且能使品红溶液褪色,则该反应的化学方程式为___________。
(3)若A、C、D、E均为化合物,E为白色絮状沉淀,且A、C、E均含有同一种元素,则该反应的离子方程式为 ___________。
Ⅱ.(1)二氧化氯是目前国际上公认的第四代高效、无毒的光谱消毒剂,它可由KClO3和H2SO4存在下与Na2SO3反应制得。请写出该反应的离子反应方程式: ___________。
(2)过碳酸钠是一种有多种用途的新型氧系固定漂白剂,化学式可表示为Na2CO33H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了还原反应的是_________。
A. MnO2 B. KMnO4溶液 C. 稀盐酸 D. Na2SO3溶液
【答案】2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑ 或 2Al + 2OH- + 6H2O = 2[Al(OH)4]- + 3H2↑ I2 + SO2 + 2H2O = 2HI+ H2SO4 Al3+ + 3 AlO2- + 6H2O = 4Al(OH)3↓ 2ClO3- + SO32- + 2H+ = SO42- + 2ClO2 + H2O D
【解析】
A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,判断为H2O;
(1)以“0.1mol/L C溶液的pH=13”为突破口,说明C为强碱性溶液,若A为短周期的金属单质,高中阶段唯有金属铝可以与强碱反应生成气体,据此推断分析;
(2)能使淀粉溶液变蓝的物质为碘单质,二氧化硫可使品红褪色,据此分析判断;
(3)考查铝三角的转化,若A、C、D、E均为化合物,E为白色沉淀,且A、C、E含有同一种元素,则A为氯化铝,C为偏铝酸钠,E为Al(OH)3、D为氯化钠;
Ⅱ.(1)二氧化氯由KClO3在H2SO4存在下与Na2SO3反应制得,则可知反应物、生成物,结合电子守恒、电荷守恒分析;
(2)Na2CO33H2O2具有Na2CO3和H2O2的双重性质,过碳酸钠只发生了还原反应,则选项中的物质具有还原性。
A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,判断为H2O;(1)若A为短周期的金属单质,0.1mol/L C溶液的pH=13,说明C为强碱性溶液,D为气态单质,判断A为Al,D为H2,该反应的离子方程式为2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑ 或 2Al + 2OH- + 6H2O = 2[Al(OH)4]- + 3H2↑,
故答案为:2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑或 2Al + 2OH- + 6H2O = 2[Al(OH)4]- + 3H2↑;
(2)若A的溶液能使淀粉溶液变蓝,A具有氧化性,C为非金属氧化物,能使品红溶液褪色,则C为二氧化硫,则A为碘,该反应的反应方程式为I2 + SO2 + 2H2O = 2HI+ H2SO4,
故答案为:I2 + SO2 + 2H2O = 2HI+ H2SO4;
(3)若A、C、D、E均为化合物,E为白色沉淀,且A、C、E含有同一种元素,则A为氯化铝,C为偏铝酸钠,E为Al(OH)3、D为氯化钠,该反应的离子方程式为Al3+ + 3AlO2- + 6H2O = 4Al(OH)3↓,
故答案为:Al3+ + 3AlO2- + 6H2O = 4Al(OH)3↓;
Ⅱ.(1)KClO3在H2SO4存在下与Na2SO3反应,SO32被氧化成SO42,由电子、电荷守恒可知该离子反应为2ClO3- + SO32- + 2H+ = SO42- + 2ClO2 + H2O,
故答案为:2ClO3- + SO32- + 2H+ = SO42- + 2ClO2 + H2O;
(6)Na2CO33H2O2具有Na2CO3和H2O2的双重性质,过碳酸钠只发生了还原反应,则选项中的物质具有还原性,只有D选项符合,
故答案为:D。


科目:高中化学 来源: 题型:
【题目】《茶疏》中对泡茶过程有如下记载:“治壶、投茶、出浴、淋壶、烫杯、酾茶、品茶……“。从化学角度考虑文中未涉及的操作方法是( )
A.溶解B.渗析C.过滤D.蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有些科学家提出硅是“21 世纪的能源”,这主要是由于作为半导体材料的硅在太阳能
发电过程中具有重要的作用。下列关于硅及其化合物的说法正确的是( )
A.水泥、玻璃、水晶饰物都是硅酸盐制品
B.高温下,可在试管内完成焦炭和石英砂(SiO2)制取硅的反应
C.光导纤维的主要成分是SiO2
D.自然界中硅元素的贮量丰富,并存在大量的单质硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.键能越小,表示化学键越牢固,难以断裂
B.两原子核越近,键长越长,化学键越牢固,性质越稳定
C.破坏化学键时,消耗能量,而形成新的化学键时,则释放能量
D.键能、键长只能定性地分析化学键的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关常见金属的说法错误的是
A.电解饱和食盐水可以获得金属钠
B.镁因在空气中形成了一薄层致密的氧化膜,故镁不需要像钠似的进行特殊保护
C.铝罐、铁罐可以盛装冷的浓硫酸、浓硝酸
D.铁、铜都是具有可变化合价的过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去粗盐中的杂质 CaCl2、MgCl2 和 Na2SO4,过程如下:
![]()
下列有关说法中,不正确的是( )
A. 除去 Mg2+的主要反应: Mg2++ 2OH-=Mg(OH)2↓
B. 试剂①一定不是Na2CO3溶液
C. 检验 SO42-是否除净:取少量滤液,加稀盐酸酸化,再加 BaCl2 溶液
D. 滤液加稀盐酸时只发生反应:H+ +OH- =H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学是指从技术、经济上设计可行的化学反应,尽可能减少对环境的负作用。下列 化学反应不符合绿色化学概念的是( )
A. 消除硫酸厂尾气排放:SO2+2NH3+H2O=(NH4)2SO3
B. 消除制硝酸厂的氮氧化物污染:NO2+NO+2NaOH=2NaNO2+H2O
C. 制 CuSO4:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D. 制 CuSO4:2Cu+O2![]() 2CuO,CuO+H2SO4(稀)=CuSO4+H2O
2CuO,CuO+H2SO4(稀)=CuSO4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L 的盐酸与50mL0.55mol/L 的 NaOH 溶液在如图所示的装置中进行中和反应。 请回答下列问题:
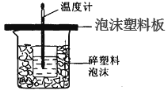
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_________;由图可知该装 置有不妥之处,应如何改正?_____。
(2)实验中改用 60 mL0.50 mol/L 的盐酸跟 50mL 0.55 mol/L 的 NaOH 溶液进行反应,与 上述实验相比,所放出的热量_____(填“相等”或“不相等”);所求中和热的数值会_____(填“相等”或 “不相等”),理由是_____。
(3)该同学做实验时有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因 是_____。
A.测量盐酸的温度后,温度计没有用水冲洗干净 B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 C.做本实验的当天室温较高 D.在量取盐酸时仰视计数
E.将 50mL0.55mol/L 氢氧化钠溶液取成了 50mL0.55mol/L 的氨水
(4)将 V1ml 1.0mol/L HCl 溶液和 V2ml 未知浓度的 NaOH 溶液混合均匀后测量并记录温 度,实验结果如下图所示(实验中始终保持 V1+V2=50mL)
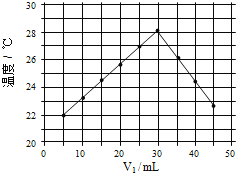
通过分析图像可知,做该实验时环境温度_____(填“高于”,“低于”或“等于”)22℃,该 NaOH 溶液的浓度约为_____mol/L。
(5)假设盐酸和氢氧化钠溶液的密度都是 1g·cm-3,又知中和反应后生成溶液的比热容 c=4.18J·g-1·℃-1。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度 t1/℃ | 终止温度 t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.2 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.3 | 20.5 | 25.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=_____(结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是( )
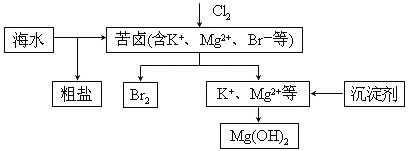
A. 向苦卤中通入Cl2是为了提取溴
B. 工业生产中常选用NaOH作为沉淀剂
C. 粗盐可采用除杂和重结晶等过程提纯
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用![]() 将其还原吸收
将其还原吸收
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com