
���� ��1��������Һϡ���������ʵ����ʵ�������������ҪŨ��ˮ��������������Ƶ���Һ���ѡ������ƿ���
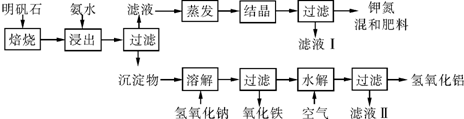
��2�����������Ϣ����ˮ�������ӷ�Ӧ���������������жϳ�����ɷ֣�
��3������ʯ����ɺ��������ƣ����ݹ�������ת����ϵ��֪����ҺI�к���K2SO4�ͷ�Ӧ���ɣ�NH4��2SO4��
��4����Ϸ����к���K2SO4����NH4��2SO4��Ҫ������ɫ�������������ҺΪBaCl2��Ba��NO3��2��Һ��Ȼ����в������Ƚ����Һ���ˣ�Ȼ��ϴ�ӳ������������ȴ����أ�����Ϊmg����174n��K2SO4��+132n[��NH4��2SO4]=m�����������ʵ���Ϊnmol����BaSO4�����ʵ���Ϊnmol������������غ��У�n��K2SO4��+n[��NH4��2SO4]=n���ݴ˼��㣮
��� �⣺��1������500mLϡ��ˮ��ÿ������39.20g��������Ҫʹ��500mL����ƿ����ҪŨ��ˮ��ÿ������250.28g���������Ϊ��$\frac{39.20g��0.5L}{250.28g}$��0.078L=78mL������Ҫ��100mL����Ͳ��
�ʴ�Ϊ��78��100��
��2������ʯ����ɺ��������ƣ������ܹ��백ˮ��Ӧ���������������������������������������������ʲ��백ˮ��ӦҲ������ˮ�����Գ�����Ϊ��Al��OH��3��Al2O3��Fe2O3��
�ʴ�Ϊ��Al��OH��3��Al2O3��Fe2O3��
��3������ʯ����ɺ��������ƣ����ݹ�������ת����ϵ��֪����ҺI�к���K2SO4�ͷ�Ӧ���ɣ�NH4��2SO4��
�ʴ�Ϊ��K2SO4����NH4��2SO4��
��4���ٻ�Ϸ����к���K2SO4����NH4��2SO4��Ҫ������ɫ�������������ҺΪBaCl2��Ba��NO3��2��Һ��
�ʴ�Ϊ��BaCl2 ��Ba��NO3��2��
��Ȼ����в������Ƚ����Һ���ˣ�Ȼ��ϴ�ӳ������������ȴ����أ�
�ʴ�Ϊ�����ˡ�ϴ�ӡ����
������Ϊmg����174n��K2SO4��+132n[��NH4��2SO4]=m�����������ʵ���Ϊnmol����BaSO4�����ʵ���Ϊnmol������������غ��У�n��K2SO4��+n[��NH4��2SO4]=n��������ã�n��K2SO4��=$\frac{��m-132n��}{42}$mol��
�ʴ�Ϊ��$\frac{��m-132n��}{42}$��
���� ���⿼��ѧ���Թ������̵����⡢���ʷ����ᴿ�Ȼ������������������뻯ѧ�����ѧ����ȣ���Ŀ�Ѷ��еȣ���Ҫѧ��������ʵ�Ļ���֪ʶ���������֪ʶ��������������


 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 32g�����ͳ����Ļ��������������ԭ����Ϊ2NA | |
| B�� | ���³�ѹ�£�22.4LCO2���еķ�����ĿΪNA | |
| C�� | 2.4g����þ�����������ᷴӦ��ת�Ƶĵ�����Ϊ0.2NA | |
| D�� | 0.1mol OH-����NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����208 kJ������ | B�� | �ų�208 kJ������ | ||
| C�� | ����93 kJ������ | D�� | �ų�93 kJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪X��һ��������ת��ΪY��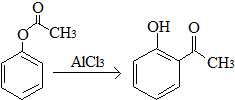 ��X��Y��Ϊͬ���칹�壬����FeCl3��Һ���� ��X��Y��Ϊͬ���칹�壬����FeCl3��Һ���� | |
| B�� | 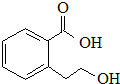 �ܷ����ķ�Ӧ�����У��ӳɷ�Ӧ��ȡ����Ӧ����ȥ��Ӧ��ˮ�ⷴӦ �ܷ����ķ�Ӧ�����У��ӳɷ�Ӧ��ȡ����Ӧ����ȥ��Ӧ��ˮ�ⷴӦ | |
| C�� | ���ۡ����������յ�ˮ����ﶼֻ��һ�� | |
| D�� | �����ʷ۾��п��������ܣ��ṹΪ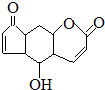 ������ˮ������Ӧ��1mol�������3molBr2������NaOH��Һ��Ӧ��1mol�������2molNaOH ������ˮ������Ӧ��1mol�������3molBr2������NaOH��Һ��Ӧ��1mol�������2molNaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ��Na2O | B�� | ֻ��Na2O2 | C�� | Na2O��Na2O2 | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �״��е���ʯ����Һ�ʺ�ɫ | B�� | �״��붹�����г������� | ||
| C�� | pH ��ֽ��ʾ�״� pH Ϊ 2��3 | D�� | ���ǽ����ڰ״���������ų� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L 0.1mol•L-1��NaHCO3��Һ��HCO3-��CO32-������֮��Ϊ0.1NA | |
| B�� | 50ml 12mol/L����������MnO2���ȣ�ת�Ƶĵ�����Ϊ0.3NA | |
| C�� | ����������CO2��Ӧʱ������0.1mol����ת�Ƶĵ�����Ϊ0.2NA | |
| D�� | �ܱ�������2molNO��1molO2��ַ�Ӧ������ķ�����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪2H2��g��+O2��g���T2H2O��g����H=-483.6kJ•mol-1���������ı�ȼ����Ϊ-483.6kJ/mol | |
| B�� | ��H����ֵ�뻯ѧ��Ӧ����ʽ�Ļ�ѧ����ϵ���� | |
| C�� | ��20.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ����������÷�Ӧ���Ȼ�ѧ����ʽΪ��NaOH��aq��+$\frac{1}{2}$H2SO4��aq���T$\frac{1}{2}$Na2SO4��aq��+H2O��l����H=-57.4 kJ•mol-1 | |
| D�� | ��֪C��s��+O2��g���TCO2��g����H1��C��g��+O2��g���TCO2��g����H2�����H1����H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͼ�ļ���ʽ��ʾ��������Ϊ��3-��-4-�һ�-7-������ | |
| B�� | ���Ϸ���ʽΪC3H8O�Ĵ������ֲ�ͬ�Ľṹ | |
| C�� | 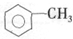 �У�����ԭ�Ӳ����ܶ���ͬһƽ���� �У�����ԭ�Ӳ����ܶ���ͬһƽ���� | |
| D�� | ����ű���������أ���ͼ��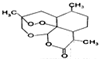 ������ʽ��C15H20O5 ������ʽ��C15H20O5 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com