
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案:
方案一 滴定法 用酸性KMnO4溶液滴定测定铁元素的含量。
反应原理:5Fe2++MnO4—+8H+===5Fe3++Mn2++4H2O
(1)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需________(填仪器名称)。
(2)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________。
A.稀硫酸 B.浓硝酸 C.稀硝酸 D.稀盐酸
(3)某同学设计的下列滴定方式中,最合理的是________(夹持部分略去)(填字母序号)。

方案二 重量法 操作流程如下:

(4)步骤②中除用H2O2外还可以使用的物质是__________________________。
(5)步骤②是否可以省略________,理由是________________________________
_______________________________________。
(6)步骤④中一系列操作依次是:过滤、洗涤、________、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量________g(用含a的代数式表示)。
(1)250 mL容量瓶 (2)A (3)B (4)氯水(等其他合理的氧化剂) (5)不能 因为Fe2+与碱反应后在空气中加热不能得到纯净的Fe2O3,故无法准确计算Fe的含量 (6)灼烧 (7)0.07a
【解析】 (1)据题意,配制一定物质的量浓度的KMnO4溶液250 mL,还需250 mL容量瓶(必须带上容量瓶的规格)。(2)由于高锰酸钾有强氧化性不能用盐酸酸化,也不用强氧化性酸(硝酸)酸化,通常用稀硫酸酸化。(3)由于高锰酸钾有强氧化性会腐蚀橡皮管,故只能用酸式滴定管(B装置)进行滴定实验。(4)除用H2O2外还可以使用氯水氧化Fe2+,不引入新的杂质离子。(5)因为Fe2+与碱反应后在空气中加热不能得到纯净的Fe2O3,无法准确计算Fe的含量,所以必须先用H2O2氧化Fe2+来实现。(6)步骤④依次将Fe(OH)3过滤、洗涤、灼烧(Fe(OH)3分解得Fe2O3、冷却、称量。(7)每片补血剂含铁元素的质量:a g÷160 g·mol-1×2×56 g·mol-1÷10片=0.07a g/片


科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第6讲化学反应速率和化学平衡练习卷(解析版) 题型:填空题
在1.0 L密闭容器中放入0.10 mol A(g),在一定温度进行如下反应:
A(g)??B(g)+C(g) ΔH=+85.1 kJ·mol-1
ΔH=+85.1 kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/100 kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为____________________。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为______________。平衡时A的转化率为__________,列式并计算反应的平衡常数K__________________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n(总)=________ mol,n(A)=________ mol。
②下表为反应物A浓度与反应时间的数据,计算:a=________。
反应时间t/h | 0 | 4 | 8 | 16 |
c(A)/(mol·L-1) | 0.10 | a | 0.026 | 0.006 5 |
分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是________________________________,由此规律推出反应在12 h时反应物的浓度c(A)为__________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第3讲两种重要的化学反应练习卷(解析版) 题型:选择题
LiAlH4是金属储氢材料又是有机合成中的常用试剂,遇水能剧烈反应释放出氢气,LiAlH4在125 ℃分解为LiH、H2和Al。下列叙述错误的是( )。
A.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
B.LiAlH4与D2O反应,所得氢气的摩尔质量为4 g·mol-1
C.1 mol LiAlH4在125 ℃完全分解,转移3 mol电子
D.LiAlH4与水反应生成三种物质时,化学方程式可表示为:LiAlH4+4H2O=Al(OH)3+LiOH+4H2↑
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第1讲物质的组成性质和分类练习卷(解析版) 题型:填空题
下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种温室气体,C的相对分子质量为78。请回答相关问题。

(1)下列对C的结构、性质推断中不正确的是( )。
A.久置于空气中会变成白色 B.具有强氧化性
C.晶体中存在离子键与非极性键 D.是一种碱性氧化物
(2)A的原子结构示意图为____________________,H的电子式为____________________,E的结构式为____________________。
(3)C和E反应生成H的离子方程式为__________________,反应中氧化剂与还原剂的物质的量之比为______。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第1讲物质的组成性质和分类练习卷(解析版) 题型:选择题
中科院化学研究所研制的晶体材料——纳米四氧化三铁,在核磁共振造影及医药上有广泛的用途,其部分生产流程如图所示。
 纳米四氧化三铁
纳米四氧化三铁
下列有关叙述不正确的是( )。
A.纳米四氧化三铁可分散在水中,其与FeCl3溶液中分散质的直径相当
B.纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病
C.在反应①中环丙胺的作用可促进氯化铁水解
D.反应②的化学方程式是6FeOOH+CO=2Fe3O4+3H2O+CO2
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第14讲物质结构与性质练习卷(解析版) 题型:填空题
2012年12月,我国成功实现歼—15飞机在“辽宁号”航母上的起降实验,建造航母平台和舰载飞机离不开如钛、物质A等材料。请回答下列问题:
(1)写出钛基态原子的核外电子排布式:___________________________。
(2)已知元素A处于第3周期,其原子的第一至第四电离能数据如表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 738 | 1 451 | 7 733 | 10 540 |
①A的元素符号为________。
②与元素A同周期的电负性最大的元素为________(填元素符号),该元素能与同周期的另一种非金属元素形成5原子分子,该分子的中心原子采用的杂化方式是________,该分子的空间构型为________。
(3)钛镁合金是制造高性能飞机的重要材料。已知钛、镁金属均采用六方最密堆积( ),下列说法正确的是________(填序号)。
),下列说法正确的是________(填序号)。
A.用钛镁合金来制造高性能飞机,主要由于其价格昂贵,制造出的飞机能卖个好价钱
B.在高温下切割金属钛不会产生任何安全事故
C.钛、镁金属晶体中,其配位数均为12
D.金属钛的熔点很高(1 668 ℃),与金属键关系不大
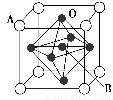
(4)钙钛型复合氧化物(如图所示)可用于制造航空母舰中的热敏传感器,该晶体以A原子为晶胞的顶点,A可以是Ca、Sr、Ba或Pb,当B是V、Cr、Mn或Fe时,这种化合物具有很好的电化学性能。用A、B、O表示钙钛型复合氧化物晶体的化学式为________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第13讲实验方案设计与评价练习卷(解析版) 题型:填空题
利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:

(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率;②________。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42—,该反应的离子方程式为________________________________________________________________________。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入稀盐酸、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应的化学方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62—
Sn2++4Cl-+2HgCl2=SnCl62—+Hg2Cl2↓
6Fe2++Cr2O72—+14H+=6Fe3++2Cr3++7H2O
①若SnCl2不足量,则测定的Fe3+量________(填“偏高”、“偏低”或“不变”,下同);
②若不加HgCl2,则测定的Fe3+量________。
(4)①可选用________(填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是________________________________________________________________________(用离子方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
实验可选用的试剂有:稀硝酸、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。
请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:________________________________________________________;
b.沉淀:__________________________________________________________;
c.分离,洗涤;
d.烘干,研磨。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第11讲有机化学基础练习卷(解析版) 题型:填空题
化合物F是合成某种抗癌药物的中间体,其合成路线如下:



(1)化合物F中的含氧官能团有羰基、________和________(填官能团名称)。
(2)由化合物D生成化合物E的反应类型是_____________________________。
(3)由化合物A生成化合物B的化学方程式是_________________________________________________________。
(4)写出同时满足下列条件的D的一种同分异构体的结构简式:____________________________。
①分子中有4种不同化学环境的氢原子;②能发生银镜反应,且其一种水解产物也能发生银镜反应;③分子中苯环与氯原子不直接相连。
(5)苯乙酸乙酯( )是一种重要的化工原料。请写出以苯、甲醛和乙醇为主要原料制备苯乙酸乙酯的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
)是一种重要的化工原料。请写出以苯、甲醛和乙醇为主要原料制备苯乙酸乙酯的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
H2C===CH2 CH3CH2Br
CH3CH2Br CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习提分训练专题11实验仪器使用及基本操作练习卷(解析版) 题型:选择题
下列有关物质检验的描述不正确的是( )。
A.检验某溶液中是否含有SO42-的方法是取少量该溶液加入BaCl2溶液,再加入稀硝酸
B.用KMnO4酸性溶液可鉴别CH3CH=CHCH3和CH3CH2CH2CH2CH3
C.用酚酞溶液或品红溶液均可鉴别NH3和SO2气体
D.取工业有机废水(无色),滴加数滴FeCl3溶液,溶液变紫色,说明此废水中含酚类物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com