
 +4H++3e-=NO+2H2O 。 已知Cu2O能使上述还原过程发生。
+4H++3e-=NO+2H2O 。 已知Cu2O能使上述还原过程发生。 _。
_。 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
 3Fe+4CO2的反应中, 是氧化剂,
3Fe+4CO2的反应中, 是氧化剂,查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
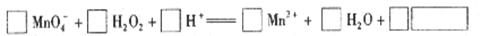

 氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)| 实验内容 | 实验方法 | 实验现象 |
| 验证氧化性 | | |
| 验证不稳定性 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2 | B.HF | C.OF2 | D.O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.全部 | B.① | C.①②③④ | D.①⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.+6 | B.+2 | C.+3 | D.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com