
【题目】
A. 不慎将浓硫酸沾到皮肤上,立即用大量的氢氧化钠溶液冲洗
B. 如果少量酒精失火燃烧,立即用水浇灭
C. 炒菜时油锅着火,立即盖上锅盖
D. 发现家中天然气泄漏,立即打开抽油烟机
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】I.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定装置如图

(1)图中A的名称是:_____________________________
(2)若实验过程中酸碱添加过慢,所得△H将________(填:偏大、偏小或者无影响)
(3)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 30.1 |
2 | 27.0 | 27.4 | 27.2 | 33.3 |
3 | 25.9 | 25.9 | 25.9 | 29.8 |
4 | 26.4 | 26.2 | 26.3 | 30.4 |
近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃).则中和热△H=_____________(取小数点后一位).
II.为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。

(4)请完成此实验设计,其中:V6=________,V8=___________
(5)该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,请分析主要原因________________________。
III.利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移取xmL一定物质的量浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂
步骤Ⅱ:移取ymL BaCl2溶液于锥形瓶中,加入xmL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用bmol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
(6)BaCl2溶液的浓度为___________mol·L-1,若步骤Ⅱ中滴加盐酸时有少量盐酸滴至锥形瓶外,Ba2+浓度测量值将______________(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体缺铁时,红细胞中血红蛋白的含量会减少,红细胞输送氧的能力也会下降,这种现象说明铁在人体具有下列哪种功能
A. 催化合成血红蛋白的反应 B. 血红蛋白的组成成分
C. 调节细胞中液体的浓度 D. 调节血浆的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙、丙、丁四种常见化合物,它们分别由H+、Na+、Al3+、Ba2+、OH-、Cl-、SO42-、HCO3-中的两种离子(离子不重复)组成,可以发生如图所示的转化。

回答下列问题:
(1)写出下列物质的化学式:甲______,丁______,A______。
(2)反应①②③中属于非氧化还原反应的有______个。
(3)向甲溶液中滴人足量丁溶液时发生反应的离子方程式为_____________。
(4)向丙溶液中滴入Fe(NO3)2溶液时发生反应的离子方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH标准溶液滴定盐酸,以下操作导致测定结果偏低的是( )
A.滴定管用待装液润洗B.锥形瓶用待测液润洗
C.滴定结束滴定管末端有气泡D.滴定时锥形瓶中有液体溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应KMnO4+HCl(浓)→MnCl2+KCl+Cl2↑+H2O中,
(1)配平上述化学方程式
(2)若生成35.5g Cl2 , 则被氧化的HCl是mol,转移的电子的物质的量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据右表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是

A. c(HCO3—)>c(ClO-)>c(OH-)
B. c(ClO-)>c(HCO3—)>c(H+)
C. c(HClO)+ c(ClO-)= c(HCO3—)+ c(H2CO3)
D. c(Na+)+ c(H+)= c(HCO3—)+c(ClO-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示. 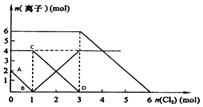
已知:
2Fe2++Br2═2Fe3++2Br﹣
2Fe3++2I﹣═2Fe2++I2
(1)Fe2+、I﹣、Br﹣的还原性由强到弱排列顺序为 .
(2)C→D代表离子浓度的变化.
(3)当通入1mol Cl2时,溶液中已发生的离子反应可表示为: .
(4)原溶液中:n(Fe2+):n(I﹣):n(Br﹣)=
(5)通入2mol Cl2时,溶液中已发生的离子反应可表示为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列说法错误的是
A.氯碱工业是电解熔融的NaCl,在阳极能得到Cl2
B.电渗析法淡化海水利用了离子交换膜技术
C.硅橡胶既能耐高温又能耐低温,广泛应用于航天航空工业
D.煤经过气化和液化等化学变化可转化为清洁能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com