
铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物。某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验。
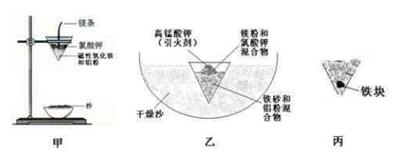
(1)取磁性氧化铁按图中甲装置进行铝热反应,现象很壮观。取少许反应生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种结果的原因,除了可能混有没反应的磁性氧化铁外,还有一个原因是 。
(2)为了克服图中甲的缺陷,改用图中乙装置进行铝热反应,主要步骤如下:
① 在一个广口容器中放进一定量的干燥细沙;
② 将一定量的铁砂和铝粉混合物装在纸漏斗中并埋入细沙里;
③ 将一定量的镁粉和氯酸钾混合物放在铝热剂上;
④ 再放上引火剂;引火反应,冷却;⑤取出反应后的铁块(如图丙)
请写出铝热反应的化学方程式:
取少许反应生成的铁块溶于盐酸,向其中滴加KSCN溶液,溶液没有出现血红色。实验中干燥细沙的主要作用是 。
(3)测定图中乙反应所得的铁块纯度,流程如下图所示。几种氢氧化物开始沉淀和沉淀完全时的pH参考19题。
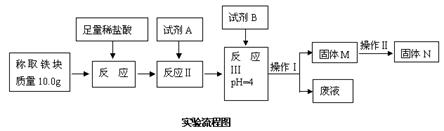
① 试剂A应选择 ,试剂B应选择 。
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水 E.MgCO3固体
② 操作Ⅰ的名称为 。操作Ⅱ的名称为 。固体M完全转化为固体N的标志是 。
③ 已知常温下Fe(OH)3的KSP=4.0×10-38,求反应Ⅲ后溶液中c(Fe3+)= mol/L
若最终红色粉末质量为14.14g,则该铁块的纯度是 。如果直接洗涤、烘干和称量固体M的质量,计算铁块的纯度,则计算结果会 (填“偏大”“偏小”或“无影响“)。原因是 。
科目:高中化学 来源: 题型:
以下一些氧化物和单质之间可发生如图所示的反应:

其中,氧化物(Ⅰ)是红棕色固体、氧化物(Ⅱ)、(Ⅲ)、(Ⅳ)在反应条件下都是气体。
(1)氧化物(Ⅰ)的化学式(分子式)是 。
氧化物(Ⅱ)的化学式(分子式)是 。
(2)反应①的化学方程式是
。
反应②的化学方程式是 。
反应③的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是( )
A.含最高价元素的化合物,一定具有强氧化性
B.阳离子只有氧化性,阴离子只有还原性
C.失电子越多,还原能力越强
D.强氧化剂与强还原剂不一定能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实的解释正确的是( )
A. 将SO2 、SO3 混合气体通入氯化钡溶液中,出现浑浊是因为生成了BaSO4沉淀
B. SO2通入溴水中,溴水褪色,是因为SO2的漂白性
C. 反应2C + SiO2  Si +2CO ,是因为碳的非金属性强于硅的非金属性
Si +2CO ,是因为碳的非金属性强于硅的非金属性
D. 在NaHCO3的溶液中滴加NaAlO2溶液中有白色沉淀生成,是因为二者发生完全水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 同一主族元素气态氢化物从上到下,其沸点逐渐升高
B.非金属单质中一定存在共价键,离子化合物中可能存在共价键
C.非极性键不可能存在于离子化合物中,由非金属元素组成的化合物中一定不存在离子键
D.含有阴离子的物质一定含有阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
有一瓶Na2SO3溶液,可能已部分氧化,某学生进行如下实验:取少量溶液,滴入Ba(NO3)2溶液 产生白色沉淀,再加入过量稀硝酸,充分振荡后仍有白色沉淀,结论正确的是
产生白色沉淀,再加入过量稀硝酸,充分振荡后仍有白色沉淀,结论正确的是
A.Na2SO3溶液已部分氧化
B.加入Ba(NO3)2溶液后生成的沉淀中一定含有BaSO4
C.加硝酸后的不溶沉淀一定为BaSO4
D.此实验能确定Na2SO3溶液是否部分氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是研究二氧化硫性质的微型实验装置。现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气。下列说法中错误的是
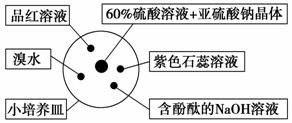
A.紫色石蕊溶液变蓝色
B.品红溶液褪色
C.溴水橙色褪去
D.含酚酞的NaOH溶液红色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
核内质子数不同,核外电子数相同的两种微粒,它们可以是( )
A.同种元素的两种离子 B.同种元素的原子和离子
C.不同种元素的离子 D.不同种元素的原子和离子
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见表,表中的“实验步骤”与“实验现象”前后不一定是对应的关系)。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”的响声,随之消失,溶液变成红色 |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究________元素性质递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等。
仪器:①________,②________,③________,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式)
| 实验步骤 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
①__________________,②____________________。
(4)实验结论:___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com