
| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |
科目:高中化学 来源: 题型:选择题
| A. | 离子交换法可以软化硬水 | |
| B. | 生产、生活使用的天然水必须经软化 | |
| C. | 硬水中含有较多Ca2+、Mg2+ | |
| D. | 加热可使暂时硬水中的Ca2+生成CaCO3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 决定元素种类的是--电子数 | |
| B. | 决定元素化学性质的是--原子的核外电子数 | |
| C. | 决定元素相对原子质量的是--中子数 | |
| D. | 决定元素周期表中原子序数的是--核电荷数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
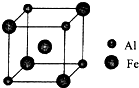 过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
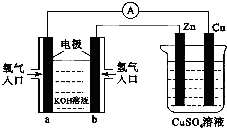
| A. | 该装置中Cu极为正极 | |
| B. | 当铜极的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L | |
| C. | b极反应的电极反应式为:H2-2e-═2H+ | |
| D. | 一段时间后锌片质量减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②⑥ | C. | ⑤⑦ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
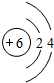 ,B与C形成的化合物的电子式为
,B与C形成的化合物的电子式为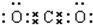 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
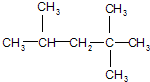 它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简
它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简 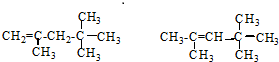 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com