

分析 KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物甲加水溶解后,溶液1中是KAl(SO4)2,沉淀B是Al2O3和Fe2O3;向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成溶液2为NaAlO2,固体C为Fe2O3,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀和溶液4为碳酸钠或碳酸氢钠,Al(OH)3受热分解生成固体D为Al2O3,电解熔融氧化铝得到O2和F为Al;向溶液1中加过量氨水,溶液1与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液3中是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的固体E是K2SO4 和(NH4)2SO4,以此来解答.
解答 解:KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物甲加水溶解后,溶液1中是KAl(SO4)2,沉淀B是Al2O3和Fe2O3;向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成溶液2为NaAlO2,固体C为Fe2O3,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀和溶液4为碳酸钠或碳酸氢钠,Al(OH)3受热分解生成固体D为Al2O3,电解熔融氧化铝得到O2和F为Al;向溶液1中加过量氨水,溶液1与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液3中是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的固体E是K2SO4 和(NH4)2SO4,
(1)D为Al2O3,固体 D 中的金属元素铝在周期表中位于:第3周期ⅢA族,
故答案为:3;ⅢA;
(2)根据上面的分析可知 Al(OH)3,沉淀的化学式为Al(OH)3,
故答案为:Al(OH)3;
(3)反应 ①的离子方程式为Al2O3+OH-═2AlO2-+H2O,②的离子方程式为 Al3++3 NH3•H2O═Al(OH)3↓+3 NH4+,
故答案为:Al2O3+OH-═2AlO2-+H2O;Al3++3 NH3•H2O═Al(OH)3↓+3 NH4+;
(4)铝和氧化铁的混合物称为铝热剂,根据方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2 Fe+Al 2O3 可知,每有 1mol 固体铝参加反应,同时有0.5mol氧化铁参加反应,
故答案为:铝热剂;0.5;
(5)铝在冷、浓硝酸反应中,发生钝化,所以铝不与冷、浓硝酸反应,
故答案为:钝化.
点评 本题考查无机物的推断,为高频考点,把握物质的性质及框图中发生的化学反应为解答的关键,侧重分析与推断能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,H2的气体摩尔体积约为22.4L | |
| B. | 标准状况下,22.4L的CO2和O2组成的混合物中,含氧原子数为2NA | |
| C. | 1mol/L CaCl2溶液中含有的氯离子数目为2NA | |
| D. | 18gNH4+中含有10NA个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Na2CO3溶液中:c(Na+):c(CO32-)=2:1 | |
| B. | 在25℃时,无论是酸性、碱性或中性溶液中,其c(H+)和c(OH-)的乘积都等于1×10-14 | |
| C. | 0.1mol/L的KOH溶液和0.1mol/L氨水中,c(OH-)相等 | |
| D. | 原电池的正极所发生的反应是氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m=p•V•w% | B. | w=$\frac{cM}{2000p}$% | C. | S=$\frac{m}{pV-m}$ | D. | c=$\frac{1000m}{VM}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3、Cl2、H3PO4 | B. | AgCl、Ba(OH)2、H2S | ||
| C. | H2SO3、NaOH、H2SO4 | D. | NH3•H2O、H2O、CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A13+、NO3-、Fe2+ | B. | SCN-、Cl-、Fe3+ | C. | HCO3-、Al3+、Cl- | D. | Na+、K+、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
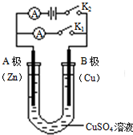 如右图所示,请按要求回答下列问题.
如右图所示,请按要求回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com