
| A.16g | B.32g | C.64g /mol | D.32g /mol |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.此电池能发出蓝色的火焰 |
| B.氧气为正极,氢气为负极 |
| C.工作时电解液一定与H2反应 |
| D.负极:2H2+4OH-—4e-===4H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.放电时储氢合金作负极 |
| B.充电时储氢合金作阴极 |
| C.1 mol LaNi5H6参加放电,能提供12 mol电子 |
| D.充电是将电能转化为化学能的过程 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2、64、24 | B.64、2、24 | C.32、50、12 | D.16、50、24 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
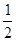 H2+NiO(OH)
H2+NiO(OH) Ni(OH)2,根据此反应式判断,下列叙述中正确的是
Ni(OH)2,根据此反应式判断,下列叙述中正确的是| A.电池放电时,电池负极周围溶液pH不断增大 | B.电池放电时,镍元素被氧化 |
| C.电池充电时,氢元素被氧化 | D.电池放电时,H2是负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
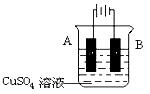
| A.CuSO4溶液 | B.CuCO3固体 | C.CuO固体 | D.Cu(OH)2固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.负极,并被氧化 | B.正极,并被还原 |
| C.负极,并被还原 | D.正极,并被氧化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2CO2+3H2O,制取二甲醚的反应如下:
2CO2+3H2O,制取二甲醚的反应如下: CO2(g)+H2(g) △H=-41.2kJ·mol-1
CO2(g)+H2(g) △H=-41.2kJ·mol-1 CH3OH(g) △H=-90.7kJ·mol-1
CH3OH(g) △H=-90.7kJ·mol-1 CH3OCH3(g)+H2O(g) △H=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H=-23.5kJ·mol-1 一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式____________________________________________________
一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式____________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com