
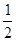 H2+NiO(OH)
H2+NiO(OH) Ni(OH)2,根据此反应式判断,下列叙述中正确的是
Ni(OH)2,根据此反应式判断,下列叙述中正确的是| A.电池放电时,电池负极周围溶液pH不断增大 | B.电池放电时,镍元素被氧化 |
| C.电池充电时,氢元素被氧化 | D.电池放电时,H2是负极 |
科目:高中化学 来源:不详 题型:填空题
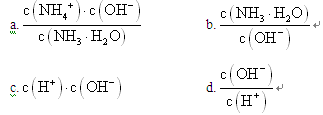
 原电池工作时电解质溶液中向正极移动的离子是_____________。
原电池工作时电解质溶液中向正极移动的离子是_____________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.工业上以黏土、石灰石和石英为主要原料来制造普通水泥 |
| B.负极的电极反应式为 2Cu + 2OH- —2e- = Cu2O + H2O |
| C.测量原理示意图中,电流方向从 Cu 经过导线流向 Ag2O |
| D.电池工作时,溶液中 OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
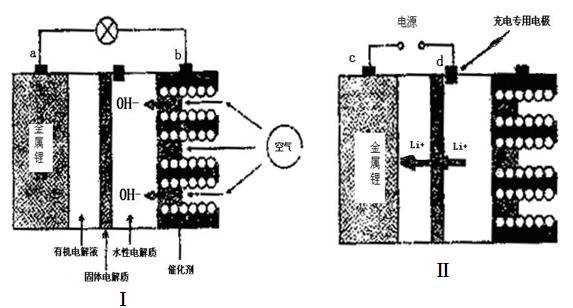
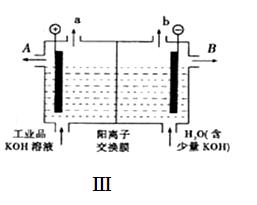
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
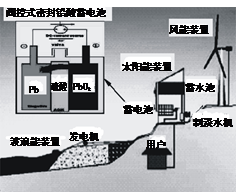
| A.图中涉及的能量转化方式只有3种 |
| B.蓄电池供电时,负极的电极反应为:Pb +SO42―-2e-=PbSO4 |
| C.储能时若充电时间过长,阳极流向阴极的气体可能是H2 |
| D.该发电工艺可实现零排放 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 分)
分)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 定比例Li2CO3和Na2CO3熔融混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。
定比例Li2CO3和Na2CO3熔融混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。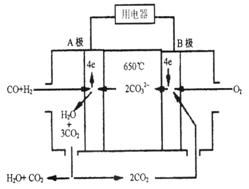
 此电源电
此电源电 解足量的CuSO4溶液,阳极产生气体0.56 L(已换算为标况),则阴极产物的质量为 g。电解后溶
解足量的CuSO4溶液,阳极产生气体0.56 L(已换算为标况),则阴极产物的质量为 g。电解后溶 液体积为1 L,溶液的pH约为 。
液体积为1 L,溶液的pH约为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电路中每流过5mol电子,肯定有5.6 L丙烷被完全氧化 |
| B.该电池的总反应是:C3H8+5O2→3CO2+4H2O |
| C.在熔融电解质中,O2-由正极移向负极 |
| D.通丙烷的电极为电池负极,发生的电极反应为:C3H8-20e-+10O2-=3CO2 +4H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com