
 如图所示,在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变.则钠和氧化汞的物质的量之比是( )
如图所示,在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变.则钠和氧化汞的物质的量之比是( )| A、1:1 |
| B、2:1 |
| C、23:216.6 |
| D、216.6:23 |
科目:高中化学 来源: 题型:
A、该反应的平衡常数表达式为K=
| ||
| B、反应前后压强不变,反应即达到平衡 | ||
| C、该反应达平衡时,A的转化率为90% | ||
| D、增加B的量,正反应速率增大,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、② | B、④ | C、⑥ | D、⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
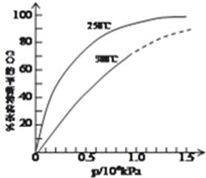 在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g)═CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示.
在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g)═CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 营养物质 | 淀粉 | 油脂 | 维生素C | 铁元素 |
| 存在、性质 | 存在于大豆、花生、绿色蔬菜中;与纤维素互为同分异构体 | 存在于动物脂肪、大豆、花生等;可溶于水,常温均呈固态 | 存在于蔬菜、水果内,可溶于水,具有很强的还原性 | 存在于动物肝脏、瘦肉等食物内;可以跟某些蛋白质结合 |
| 在人体内的 主要作用 | 用于水解形成葡萄糖,为人体提供能量 | 保温、缓冲,帮助脂溶性维生素吸收,储存能量及必要时氧化释放能量 | 清除导致人体衰老的自由基,促进铁元素吸收等 | 用于合成甲状腺素,促进智力发育 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com