
 =0.2mol,设混合物中含有xmolFe,ymolZn,
=0.2mol,设混合物中含有xmolFe,ymolZn,
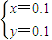 ,
, =46.3%,
=46.3%,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(6分)今有Fe和Zn的混合物12.1g,与足量的稀盐酸反应,共放出H24.48L(标准状况)。求:
(1)原混合物中Fe的质量分数。
(2)消耗HCl的物质的量。
查看答案和解析>>
科目:高中化学 来源:2010年福建省福州市八县(市)协作校第一学期期中联考高一化学试卷 题型:填空题
(6分)今有Fe和Zn的混合物12.1g,与足量的稀盐酸反应,共放出H2 4.48L(标准状况)。求:
(1)原混合物中Fe的质量分数。
(2)消耗HCl的物质的量。
查看答案和解析>>
科目:高中化学 来源:2010年福建省福州市八县(市)协作校第一学期期中联考高一化学试卷 题型:填空题
(6分)今有Fe和Zn的混合物12.1g,与足量的稀盐酸反应,共放出H2 4.48L(标准状况)。求:
(1)原混合物中Fe的质量分数。
(2)消耗HCl的物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:
今有Fe和Zn的混合物12.1g,与足量的稀盐酸反应,共放出H2 4.48L(标准状况)。求:
(1)原混合物中Fe的质量分数。
(2)消耗HCl的物质的量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com