
 ���л�ѧʵ�����ע�ⰲȫ������˵������ȷ������ǣ�������
���л�ѧʵ�����ע�ⰲȫ������˵������ȷ������ǣ�������| A�� | �٢ڢۢ� | B�� | �٢ڢ� | C�� | �٢ڢ� | D�� | �٢ڢۢܢ� |
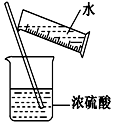
���� �ٸ��ݿ�ȼ�������������Ϻ��ȼ���ܷ�����ը���з����жϣ�
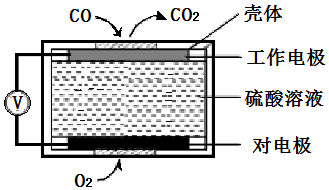
��COβ��Ӧ��ȼ������
����˿��������ȼ������������������
����������ԭ����ͭʱ���ȼ�����ͨ������������ȵ��������Ϳ����Ļ�����壻
��ϡ��Ũ����ʱӦ��Ũ����ע��ˮ�У�
��� �⣺�ٿ�ȼ�������������Ϻ��ȼ���ܷ�����ը���������п�ȼ�ԣ�Ϊ��ֹ��ȼʱ������ը����ȼǰ����Ҫ�ȼ�����������Ĵ��ȣ�����ȷ��
��CO���������壬���ᡢ��ξ����ܷ�Ӧ����Ӧ��COβ�����е�ȼ����������ȷ��
����ʢO2�ļ���ƿ�н�����˿ȼ��ʵ��ʱ�������ڼ���ƿ�ײ�����һ��ɳ�ӣ���ֹ��ȼ�����ɵ���������������ը�Ѽ���ƿ������ȷ��
����������ԭ����ͭʱ���ȼ�����ͨ������������ȵ��������Ϳ����Ļ�����壬������ը���ʴ���
��ϡ��Ũ����ʱӦ��Ũ����ע��ˮ�У������������Һ�ķɽ����ʴ���
��ѡB��
���� ���⿼���˳�����ѧʵ������������жϣ��淶ʵ����������DZ���������ȫ��ǰ�ᣬ���ܱ���ܶ�Σ�յķ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ���� | �� | �� | �� | �� |
| A | 2mol | 1mol | 2mol | 1mol |
| B | 1mol | 1mol | 2mol | 2mol |
| A�� | A��ת���ʣ����������ң��� | B�� | A��ת���ʣ������ң������� | ||
| C�� | B��ת���ʣ������ף��ң��� | D�� | B��ת���ʣ��ף��ң������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4.2 g CO | B�� | 6.6 g CO2 | C�� | 8 g SO2 | D�� | 9.8 g H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
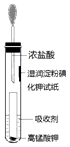 �������˲����㣬�Ҿ���һ����Σ���ԣ�Ŀǰ��������������Խ��������Ʒ���������ش�
�������˲����㣬�Ҿ���һ����Σ���ԣ�Ŀǰ��������������Խ��������Ʒ���������ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| ʵ����� | 1 | 2 | 3 | 4 |
| ����NaOH��Һ�������mL�� | 20.05 | 20.00 | 18.80 | 19.95 |
| ��ƿ����Һ | �ζ�������Һ | ѡ��ָʾ�� | ѡ�õζ��� | |
| A | �� | �� | ʯ�� | ���ң� |
| B | �� | �� | ���� | ���ף� |
| C | �� | �� | ��̪ | ���ף� |
| D | �� | �� | ��̪ | ���ң� |
| ����Ũ�ȣ�mol•L-1�� | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��С�������ݻ� | |
| B�� | �����������ݻ����䣬ͨ��ϡ������ | |
| C�� | ����������ѹǿ���䣬ͨ��ϡ������ | |
| D�� | ��ʱ�����ɵ�NH3�����ȥ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com