
| 10-3.10-3 |
| 0.1 |
| 10-3.10-3 |
| 0.1 |
|
|
| 10-14 |
| 10-5 |


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
 )具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
)具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )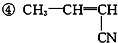 ⑤CH3-CH═CH2.
⑤CH3-CH═CH2.| A、③⑤ | B、②③ | C、①③ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)标准状况下,CO2分子数为6.02×1023,CO2的物质的量为
(1)标准状况下,CO2分子数为6.02×1023,CO2的物质的量为查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 碳、氮、氧是地球上丰富的元素.
碳、氮、氧是地球上丰富的元素.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com