
【题目】根据所学知识填空。
(1)工业制备硝酸流程如图1: 
①上述尾气中的NO一定条件下可与氨气反应转化为氮气,则该反应的化学方程式为 .
②某同学在实验室蒸馏含有Mg(NO3)2的稀硝酸制取浓硝酸,除导管、酒精灯、牛角管、锥形瓶、温度计、蒸馏烧瓶外,还需的玻璃仪器有 .
(2)某兴趣小组采用如图2装置制取并探究SO2气体的性质.
①下列实验方案适用于如图2所示装置制取所需SO2的是(填序号)
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4
②将SO2通入到以下有颜色的溶液中,溶液的颜色均褪去,其中属于漂白的是 .
A.紫色高锰酸钾溶液 B.氯水 C.品经溶液 D.红色酚酞溶液
③证明c中生成气体是SO2 , d中加入品红溶液后,打开活塞b,反应开始,待d中溶液后,再(填实验的操作)试管d中的溶液,颜色又恢复,证明气体是SO2 .
④指导老师指出应增加一尾气吸收装置,并帮助同学们设计了如装置如图3,其中合理的是(填序号)
【答案】
(1)6NO+4NH3 ![]() 5N2+6H2O;冷凝管
5N2+6H2O;冷凝管
(2)B;C;红色褪去;加热;A
【解析】解:(1.)①NO一定条件下可与氨气反应转化为氮气,结合原子守恒配平书写得到化学方程式为:6NO+4NH3 ![]() 5N2+6H2O,
5N2+6H2O,
所以答案是:6NO+4NH3 ![]() 5N2+6H2O;
5N2+6H2O;
②某同学在实验室蒸馏含有Mg(NO3)2的稀硝酸制取浓硝酸,除导管、酒精灯、牛角管、锥形瓶、蒸馏烧瓶、温度计外,还需的玻璃仪器有:冷凝管;所以答案是:冷凝管;
(2.)①实验室用Na2SO3 固体与浓硫酸反应制备二氧化硫气体,而如图所示装置没有加热,则不能用浓硫酸和铜反应制备,
所以答案是:B;
②A.SO2与紫色高锰酸钾溶液发生氧化还原反应,溶液的颜色均褪去; B.SO2与氯水发生氧化还原反应,溶液的颜色均褪去; C.SO2使品红溶液褪色,是因为二氧化硫有漂白性; D.SO2溶于水,具有酸性,所以红色酚酞溶液褪色,故选C;
③若要证明c中生成的气体是SO2 , 依据二氧化硫能使品红试液褪色,加热恢复红色;d中加入品红溶液后,打开活塞b,反应开始,待d中溶液红色褪去,再加热试管d中的溶液,颜色又恢复,证明气体是SO2 , 所以答案是:红色褪去; 加热;
④增加一尾气吸收装置防止污染性气体排放到空气中,装置需要很好地吸收气体,又能防止倒吸,BC易发生倒吸,D硫酸不能吸收二氧化硫,故选:A.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】等体积混合0.1molL﹣1的盐酸和0.06molL﹣1的Ba(OH )2溶液,不考虑体积效应,即认为混合溶液的体积等于进行混合的两溶液体积之和,溶液的pH值等于( )
A.2.0
B.12.3
C.1.7
D.12.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.pH<7的溶液一定是酸性溶液
B.室温时,pH=5的溶液和pH=3的溶液相比,前者c(OH﹣)是后者的100倍
C.室温下,每1×107个水分子中只有一个水分子发生电离
D.HCl溶液中无OH﹣ , NaOH溶液中无H+ , NaCl溶液中既无OH﹣也无H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】社会实践活动中,课外兴趣小组对某钢铁厂的铁矿石样品和钢样进行实验、分析、计算,了解了该钢铁厂生产原料、产品的相关信息。下面请你根据他们的实验帮助计算回答:
取该厂的某钢样粉末28.36 g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3 g白色沉淀。
(1)计算此钢样粉末中铁和碳的质量之比。
(2)再取三份不同质量的钢样粉末分别加到50 g质量分数相同的硫酸中,充分反应后,测得的实验数据如下表所示:(标准状况下,2 g H2的体积为22.4 L)
实验序号 | Ⅰ | Ⅱ | Ⅲ |
加入钢样粉末的质量 / g | 2.836 | 5.672 | 8.508 |
生成气体的体积(标准状况)/ L | 1.12 | 2.24 | 2.80 |
请根据表中数据计算硫酸中H2SO4的质量分数。
(3)若在实验Ⅱ中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少? (用含m的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率,减少环境污染. 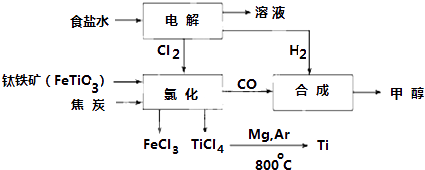
请回答下列问题:
(1)Fe位于元素周期表中第周期,第族.
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去).
[A] ![]() [B]
[B] ![]() [C]
[C]
试回答:
(1)若X是强氧化性单质,则A不可能是 .
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示) .
(3)A还可以是氨气,氨气分子的空间构型是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是。
(2)实验过程中,装置B中产生的现象是 , 这个现象说明SO2具有的性质是。
(3)装置C中Na2S溶液在空气中不易保存,时间长了会变浑浊,原因是(用离子方程式表示)。
(4)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象。
(5)如果把分液漏斗中的浓硫酸换作浓HNO3 , 对此实验是否有影响(填“是”或“否”),请说明你的理由。
(6)工业上用黄铜矿(CuFeS2)冶炼铜,副产品中也有SO2 , 冶炼铜的反应为8CuFeS2 + 21O2 ![]() 8Cu + 4FeO + 2Fe2O3 + 16SO2 , 若CuFeS2中Fe的化合价为+2,反应中被还原的元素是(填元素符号)。当生成0.8mol铜时,此反应转移的电子数目是。
8Cu + 4FeO + 2Fe2O3 + 16SO2 , 若CuFeS2中Fe的化合价为+2,反应中被还原的元素是(填元素符号)。当生成0.8mol铜时,此反应转移的电子数目是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com