
草酸(H2C2O4)是二元弱酸,草酸氢钠溶液显酸性。常温下向10mL 0.01mol/L NaHC2O4溶液中滴加0.01mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是 ( )
A.V(NaOH) = 0时,c(H+)=1×10—2mol/L
B.V(NaOH) <10mL时,一定存在c(Na+)=c(C2O42-)+c(HC2O4- )
C.V(NaOH) = 10 mL时,c(H+) = 1×10—7 mol/L
D.V(NaOH)>10 mL时,c(Na+)>c(C2O42-)>c(HC2O4- )
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
下列事实与胶体性质无关的是
A.可用半透膜除去淀粉溶液中的少量NaCl
B.黄河入海口容易形成沙洲
C.将植物油倒入水中用力搅拌可形成油水混合物
D.一束平行光线通过蛋白质溶液,从侧面可以看到一条光亮的通路
查看答案和解析>>
科目:高中化学 来源: 题型:
在无色透明的强酸性溶液中可以大量共存的离子组是( )
A.Na+、NO3-、Mg2+、Cl- B.Na+、CO32-、NO3-、Ca2+
C.K+、Cl-、SO42-、Cu2+ D.Ba2+、Cl-、K+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.1铁和铝的混合粉末溶于200mL、5mol/L的盐酸中,反应后盐酸的浓度变为4.6mol/L,若忽略溶液体积的变化,试计算:
(1)原混合物中铁和铝的质量各为多少?
(2)反应后产生的气体在标准状况下的体积多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是 ( )
A.某溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,该溶液pH一定为14-a
B.0.1mol/L的KHA溶液,其pH=10,c(K+)>c(A2-)>c(HA-) >c(OH-)
C.将0.2 mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:c(HA)>C(Na+)>c(A-)
D.等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:
3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是 ( )
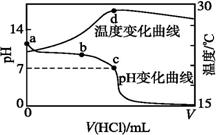
A.a点由水电离出的c(H+)=1.0×10-14 mol·L-1
B.b点:c( NH4+)+c(NH3·H2O)=c(Cl-)
C.c点:c(Cl-)=c(NH4+)
D.d点后,溶液温度略有下降的主要原因是
NH3·H2O电离吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g)  2NH3(g) △H= -92.4 kJ/mol 据此回答以下问题:
2NH3(g) △H= -92.4 kJ/mol 据此回答以下问题:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是 (填序号)。
①反应压强为20Mpa~50Mpa ②500℃的高温 ③铁触媒作催化剂
④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中。
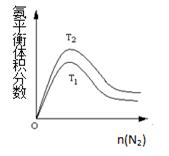 (2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度)。则T2 T1(填>、=、<),
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度)。则T2 T1(填>、=、<),
判断的依据是: 。(3分)
(3)合成氨气所需的氢气可以由水煤气分离得到。
涉及反应信息如下:
反应一:C(s)+H2O(g)  H2(g)+CO(g) 平衡常数K1
H2(g)+CO(g) 平衡常数K1
反应二:CO(g)+H2O(g)  H2(g)+CO2(g) 平衡常数K2
H2(g)+CO2(g) 平衡常数K2
① K1的表达式:K1= 。(3分)
②将一定量的H2O(g)和CO(g)分别通入到体积为1L的密闭容器中,在不同条件下进行反应,得到以下三组数据:
| 实验组别 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 2 | 900 | 0.5 | 1 | 0.2 | 0.8 | 3 |
| 3 | T | a | b | c | d | t |
(Ⅰ)实验1中,用CO2表示反应开始到平衡的平均反应速率为 。
(Ⅱ)在实验3,当a=0.5、b=1时,要使c、d数据与实验2相同,且t<3,可以采取的措施为 (填序号) (3分)
A.其它条件不变温度T<900℃ B.其它条件不变温度T>900℃
C.充入一定量氖气 D.使用高效催化剂
(Ⅲ)对于反应二,当升高温度时K2 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
把Ba(OH)2溶液滴入明矾溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( )
A.Al3+ B.Al(OH)3 C.AlO2- D.Al3+和Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、X均为中学化学常见物质一定条件下它们有如图转化关系(其他产物已略去).下列说法正确的是
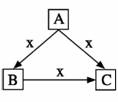
A.若X为Fe,则C可能为Fe(NO3 )2
B.若X为KOH溶液,则A可能为Al
C.若X为O2,则A可为有机物乙醇,也可为非金属单质硫
D.若A、B、C均为焰色反应呈黄色的化合物,则X一定为CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com