
【题目】下列关于如图所示实验的说法正确的是
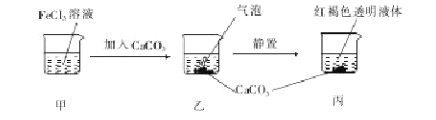
A.甲、丙两液体均可产生丁达尔现象
B.乙中产生的气泡使BaCl2溶液变浑浊
C.若忽略溶液体积的变化,则烧杯中c(Cl-)不变
D.若将CaCO3换成CaSO4,也可得到相同的实验现象
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,X的最外层电子数比内层电子数多1,Y是短周期元素中金属性最强的元素,Z的最外层电子数与次外层电子数之比为3:4。
(1)Y的原子结构示意图为_____________。
(2)W的最高价氧化物对应水化物的化学式为__________。Y和W形成的化合物的电子式为______。
(3)隔绝空气加热,Y单质可与X的氧化物反应制备X单质,该反应的化学方程式为______________
(4)0.2mol化合物Z2W2与水反应转移电子的物质的量为0.3mol,生成一种能使品红溶液褪色的气体,该反应过程中只有一种元素化合价发生变化,该反应的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、在金刚石、CS2、N2、C2H4、H2O2、金属Fe 等六种晶体中:
(1)以非极性键结合的非极性分子是______________;
(2)通过非极性键形成的原子晶体是______________;
(3)含有极性共价键和非极性共价键的非极性分子是______________;
(4)固态和熔融状态下都能导电的晶体是______________;
Ⅱ、C和Si元素在化学中占有极其重要的地位.
(1)CO2属于______________晶体,熔化时克服的微粒间作用力是______________;SiO2属于______________晶体,熔化时克服的微粒间作用力是______________;所以熔点CO2 ______________SiO2(填“<”、“=”或“>”).
(2)SiO2晶体中每个硅与______________个O相连,每个氧与______________Si相连.
(3)石墨晶体中,层内形成正六边形的平面网状结构,试分析层内每个正六边形占有的碳原子数为___________个。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是__________________。
(2)已知0.2 mol KBrO3在反应中得到1 mol电子生成X,则X的化学式为_____________。
(3)根据上述反应可推知__________________。
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:(注:请一定用单线桥表示,凡是用双线桥表示的不得分)
![]()
![]()
(5)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
(1)当n=2时,写出AB2的电子式______________,分子中有______________个σ键,______________个π键。
(2)当n=3时,A单质形成的晶体属于______________晶体;
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是______________(用元素符号表示)。
(4)已知某红紫色络合物的组成为CoCl35NH3H2O。该络合物中的中心离子钴离子在基态时核外电子排布简式为______________;
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为______________。
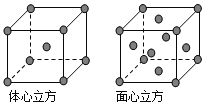
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料。以含镍(Ni2+)废液为原料生产NiOOH的一种T艺流程如下:
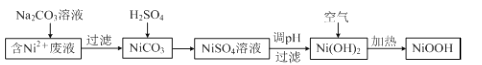
(1)加入Na2CO3溶液时,确认Ni2+已经完全沉淀的实验方法是 。
过滤时需用到的玻璃仪器有烧杯、 。
(2)写出碳酸镍与稀硫酸反应的离子方程式: 。
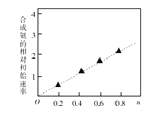
(3)硫酸镍溶液可用于制备合成氨的催化剂CoNi(1-n) Fe2O4。 如图表示在其他条件相同时合成氨的相对初始速率随催化剂中w值变化的曲线,由图分析可知Co2+、Ni2+两种离子中催化效果更好的是 。
(4)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式:__ _。
(5)若加热不充分,制得的NiOOH中会混有Ni(OH)2,其组成可表示为xNiOOHyNi(OH)2。现称取9.18g样品溶于稀硫酸,加入100mL1.0mol/LFe2+标准溶液,搅拌至溶液澄清,定容至200mL。取出20.00mL,用0.010molL﹣1 的KMnO4标准溶液滴定,用去KMnO4标准溶液20.00mL,试通过计算确定x:y= 。[已知反应(未配平):NiOOH+Fe2++H+=Ni2++Fe3++H2O,Ni2+ +MnO4 -+H+![]() Ni3++ Mn2++H2O]
Ni3++ Mn2++H2O]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物学家借助新的显微技术,成功观察到小于200纳米的粒子。下列分散系中,分散质粒子半径最小的是( )
A.雾 B.蛋白质溶液 C.石灰乳 D.KNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下图所示为实验室常见气体制备、净化、干燥、收集和性质等实验所用到的部分仪器,某校化学兴趣小组利用这些仪器进行实验探究,请你参与实验并完成有关问题:
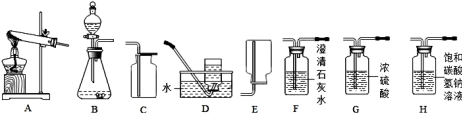
(1)甲组同学用加热高锰酸钾的方法制取氧气,应选择的发生装置为 (填字母序号);若他们选用D装置来收集O2,当气体收集满后,从水槽中取出集气瓶的操作为 。
(2)乙组同学以石灰石和稀盐酸为原料,制备并收集一瓶干燥、纯净的二氧化碳气体,按要求设计实验装置、连接仪器、并检验装置的气密性、所选仪器的连接顺序应为: → → → ;请用离子方程式表示H瓶中饱和NaHCO3溶液的作用: ;若将少量二氧化碳气体通入澄清石灰水中,发生反应的离子方程式为 。
Ⅱ.某校化学实验室有四瓶失去标签的溶液,分别标为A、B、C、D,已知它们是碳酸钠溶液、氯化钡溶液、硫酸钠溶液和稀盐酸中的一种。该校化学兴趣小组的同学进行以下实验探究来鉴别这四种溶液。
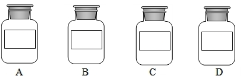
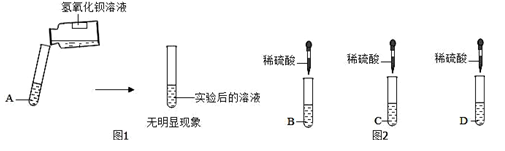
(3)丙同学的实验操作如图1所示,由此你推断该同学认为A一定不是 ;然后他再接着向实验后的混合溶液中滴加酚酞试液,发现混合溶液由无色变为红色,则丙同学得出结论:A一定是氯化钡溶液。
(4)丁同学则不同意丙同学的结论,你认为丁同学的理由是 ;于是丁同学另取少量A于试管中,向其中滴加一种试剂为 (注:只能从下列备选试剂中选择一种!),根据所选试剂他应该观察到的明显现象为 ;
A.饱和食盐水 B.K2CO3溶液 C.蒸馏水 D.紫色石蕊试液
由此证明了丙同学的结论是错误的;同时也确定了A的成分。
(5)戊同学的实验操作如图2所示,实验时观察到C中产生气泡,D中产生白色沉淀。写出D中发生反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com