
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活的事例中发生了氧化还原反应的是 。
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用如图表达。
试写出有水参加、水为还原剂且为类型Ⅳ的一个化学方程式: 。
(3)NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2反应的离子方程式是:
①请补充完整,配平方程式并标出电子转移的方向和数目。
②某同学称取了7.9 g KMnO4,固体,欲配制100 mL溶液。回答下列问题:
该实验中,使用容量瓶时要检查是否漏水,其操作是 。
③不规范的实验操作会导致实验结果的误差。下列操作会使实验结果偏小的是 (填序号)。
A.在溶解过程中有少量液体溅出烧杯外
B.定容时仰视容量瓶上的刻度线
C.定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线
④某同学用上述配好的KMnO4溶液滴定未知浓度的NaNO2溶液:取20 mL未知浓度的NaNO2溶液于锥形瓶;取上述配好的KMnO4溶液于________(填“酸式”或“碱式”)滴定管,滴定完成后消耗KMnO4溶液10 mL,则NaNO2溶液的浓度为________________。
(1)D (2) 2F2 + 2H2O =" 4HF" + O2
(3)① 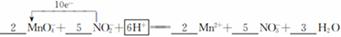 ②往容量瓶中加入少量的蒸馏水,盖上瓶塞,看瓶塞处是否漏水,放正,瓶塞旋转180度,重新倒置,看是否漏水 ③ABC ④酸式 0.625mol·L–1
②往容量瓶中加入少量的蒸馏水,盖上瓶塞,看瓶塞处是否漏水,放正,瓶塞旋转180度,重新倒置,看是否漏水 ③ABC ④酸式 0.625mol·L–1
解析试题分析:(1)A、B、C都是物理变化,D燃烧是化学反应,且都属于氧化还原反应。(2)四种基本反应类型 中属于氧化还原反应的只有置换反应,水作还原剂,则只能氧元素被氧化,联系氟气与水的反应可写出化学方程式:2F2 + 2H2O =" 4HF" + O2。(3)①反应在酸性溶液中进行,所以方框中应补写H+;Mn的化合价降低5(+7到+2),N元素的化合价升高2(+3到+5),所以MnO4–和Mn2+都配2,NO2–和NO3–都配5,根据电荷守恒,H+配6,根据原子个数守恒H2O配3。②检查容量瓶是否漏水的方法为:往容量瓶中加入少量的蒸馏水,盖上瓶塞,倒置,看瓶塞处是否漏水,正立,瓶塞旋转180度,重新倒置,看是否漏水。③A、少量液体溅出烧杯外,造成溶质的物质的量减小,所配溶液浓度偏小;B、定容时仰视容量瓶上的刻度线,则加水过量,所配溶液浓度偏小;C、“又加入少量水至刻度线”会造成水量增加,溶液浓度偏小。故选ABC。④酸化KMnO4溶液有强氧化性,能氧化橡皮管,所以不用碱式滴定管而用酸式滴定盛装KMnO4溶液;从离子方程式可知KMnO4与NaNO2按2:5的物质的量之比反应,KMnO4的浓度为: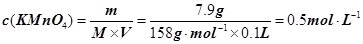 ,则NaNO2溶液的浓度为:
,则NaNO2溶液的浓度为: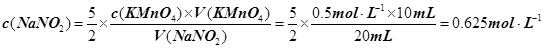 。
。
考点:考查氧化还原剂反应的应用、化学方程的书写与配平、溶液的配制及溶液浓度的测定。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:填空题
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成成分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用如图表达。
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________________________,
其中水为_______剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
_____CuO+_____NH4Cl _____Cu+_____CuCl2+N2↑+_____H2O。
_____Cu+_____CuCl2+N2↑+_____H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是_______(填元素名称),氧化剂是_______(填化学式)。
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10,10C+P4O10=P4+10CO。每生成1 mol P4时,就有_______mol电子发生转移。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为________________________;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式为______________________。
(2)请以FeSO4溶液、KI溶液、氯水、2% KSCN为试剂证明I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。
| 实验步骤 | 预期现象与结论 |
| 步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 | 现象:溶液变成黄色。 结论: 。 |
| 步骤2:__________________________ __________________________________ | 现象: ; 结论: |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
用双桥法分析下列反应,并指出氧化剂和还原剂。
(1)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(2)2H2 + O2 ==2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
2KMnO4+16HCl=2MnCl2+5Cl2↑+8H2O+2KCl,在这个反应中,氧化剂是 ,氧化产物是 ,用双线桥标出电子的转移方向和数目 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2 NaClO3+4 HCl="2" ClO2↑+ Cl2↑+ 2 NaCl+2 H2O
方法二:2 NaClO3+H2O2+H2SO4=2 ClO2↑+ O2↑+Na2SO4+2 H2O
(1)方法一的离子方程式为 ;
(2)方法二中被氧化的物质是 ,若反应中有0.1mol电子转移,则产生的ClO2气体在标准状况下的体积为 L;在下面的化学式上标出电子转移的方向和数目
2 NaClO3+H2O2+H2SO4=2 ClO2↑+ O2↑+ Na2SO4+2 H2O
(3)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO—与ClO3—的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为 ;
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知反应:3NO2+H2O═2HNO3+NO,回答下列问题:
(1)该反应的离子方程式为 .
(2)氧化剂与还原剂的质量比为 .
(3)在标准状况下,3.36L NO2与H2O完全反应转移的电子数目为 .
(4)用双线桥标出该反应中电子转移的方向和数目 .
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
过氧化氢(H2O2,O的化合价为-1价)俗称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。研究下列涉及H2O2的反应,完成下列各题:
A.Ag2O+ H2O2=2Ag+O2 ↑+ H2O
B.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)写出一个H2O2既体现氧化性又体现还原性的化学反应方程式 。
(2)将下列物质:H2O2、K2SO4、MnSO4、H2SO4、KMnO4、O2的化学式分别填在空白处组成一个不需配平的化学方程式: + +______ → + + + H2O
①该反应中的还原剂是 。
②该反应中,发生还原反应的元素是 。
(3)氧化性:KMnO4_____K2CrO4(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
高锰酸钾可用于除去地下水的硫化氢异味的原理是生成的硫和二氧化锰等沉淀物可过滤除去。水体呈弱酸性时,高锰酸钾的还原产物是MnO和MnO2,且MnO和MnO2的物质的量比为3:1。
(1)写出并配平上述化学方程式,标出电子转移方向与数目。
KMnO4 + H2S +H2SO4 →
在处理饮用水时,活性炭应在高锰酸钾反应结束后投加,否则会发生反应:
KMnO4 + C +H2O →MnO2 + X +K2CO3 (未配平)
(2)X的化学式为__________。
(3) 1mol氧化剂被______(填“氧化”或“还原”)时,生成_____mol氧化产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com