
分析 氢氧化钙与二氧化碳反应生成白色的碳酸钙沉淀Ca(OH)2+CO2═CaCO3↓+H2O,据此检验二氧化碳是否存在;若二氧化碳过量,生成的白色沉淀碳酸钙与二氧化碳反应生成可溶性的碳酸氢钙.
解答 解:实验室中检验CO2气体最方便的方法是将CO2气体通入饱和的澄清石灰水中,相应的离子反应方程式为:CO2+Ca2++2OH-═CaCO3+H2O;若继续通入过量的CO2气体,碳酸钙沉淀会与二氧化碳反应生成碳酸氢钙,沉淀被溶解,反应的离子方程式为:CaCO3+CO2+H2O═Ca2++2HCO3-,
故答案为:CO2+Ca2++2OH-═CaCO3↓+H2O,沉淀溶解;CaCO3+CO2+H2O═Ca2++2HCO3-.
点评 本题考查了离子方程式的书写,题目难度不大,明确离子方程式的书写方法以及反应原理是解答关键,试题培养了学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:解答题
 营养均衡有利于身体健康.某品牌高钙梳打的配料标签如图所示.
营养均衡有利于身体健康.某品牌高钙梳打的配料标签如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
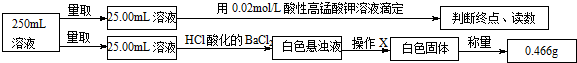
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 10.32 | 10.02 | 9.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Y<Q<W | |
| B. | ZX3可使紫色石蕊溶液变蓝 | |
| C. | X、Z、Q三种元素可组成离子化合物或共价化合物 | |
| D. | X2Q2、Y2X6两种分子中含有的电子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、W、U的最高价氧化物对应的水化物酸性由强到弱的顺序为:U>W>X | |
| B. | Y、Z元素的单质作电极,在氢氧化钠溶液中构成原电池,Z电极上产生大量气泡 | |
| C. | 室温下,0.05.mol•L-1U的气态氢化物的水溶液的pH>1 | |
| D. | Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com