
(12分)在一体积不变的密闭容器中进行如下反应:2X(g)+Y(g)  2W(g);反应前按n(X)∶n(Y)=3∶1加入反应物,反应过程中W的物质的量随时间的变化如图所示。
2W(g);反应前按n(X)∶n(Y)=3∶1加入反应物,反应过程中W的物质的量随时间的变化如图所示。
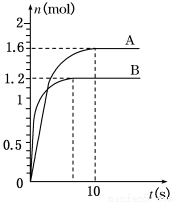
(1)分析曲线A和B的不同,可能是以下_____ ___原因造成的。
A.是否使用催化剂 B.反应温度不同
C.外界的压强不同 D.初始充入的反应物的物质的量不同
(2)该反应的化学平衡常数为K,比较K500℃___ _____K600℃(填“>”、“<”或“=”)。
(3)如果曲线B达到平衡时,体系的压强为反应前的85%,当容器的体积为1 L时,计算:曲线A从开始达到平衡,X的反应速率v(X)为____________。起始时加入Y的物质的量为______________mol。不通过计算能否判断出X、Y转化率是否相同_________________(填“能”或“否”)。
(4)说明该反应已达到平衡状态的是_________________。
A.v正(W)=v逆(W) B.c(X)=c(W)
C.气体的平均摩尔质量不变 D.气体的密度保持不变
科目:高中化学 来源:2016届安徽省安庆市高三上学期第一次质检化学试卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是
A.打开汽水瓶有气泡从溶液中冒出
B.实验室用排饱和食盐水法收集氯气
C.合成氨工厂采用增大压强以提高原料的转化率
D.2NO2(g)  N2O4(g)的平衡体系中,加压缩小体积后颜色加深
N2O4(g)的平衡体系中,加压缩小体积后颜色加深
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上学期10月月考化学试卷(解析版) 题型:填空题
(8分)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
醋酸 | 碳酸 | 亚硫酸 |
Ka= 1.75×10-5 | Ka1= 4.30×10-7 Ka2 = 5.61×10-11 | Ka1= 1.54×10-2 Ka2 = 1.02×10-7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = 。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱: > > 。
(3)下图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化
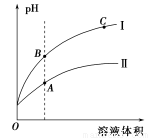
①图像中,曲线I表示的酸是 (填化学式)。
②A、B、C三点中,水的电离程度最大的是 (填字母)。
查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水,得到的溶液密度为q g/cm3(此过程中无溶质析出),物质的量浓度为c mol·L﹣1.则溶质的相对分子质量为
A.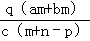 B.
B.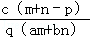
C.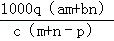 D.
D.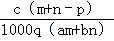
查看答案和解析>>
科目:高中化学 来源:2016届江西省吉安市高三上学期第一次月考化学试卷(解析版) 题型:推断题
A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示.
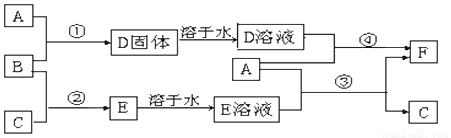
请回答:
(1)写出B物质的化学式: .
(2)写出第③步反应的化学方程式为 .
(3)第④步反应的离子方程式是 .
(4)写出SO2在水中与B反应的离子方程式 .
(5)F溶液中滴入NaOH溶液可能产生的实验现象是 .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期第一次月考化学试卷(解析版) 题型:选择题
中和pH相同、体积相同的H2SO4、HCl和CH3COOH溶液,耗用同一浓度的NaOH溶液,体积分别为V1、V2和V3,则V1、V2和V3的关系正确的是
A.V1>V2=V3 B.V3>V2=V1
C.V1>V2>V3 D.V1=V2=V3
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期第一次检测化学试卷(解析版) 题型:实验题
(12分)实验室用固体烧碱配制500 mL 0.1 mol·L―1的NaOH溶液。
(1)需称量____________g的烧碱固体,它应该盛放在____________ 中进行称量。
(2)配制过程中,不需要使用的仪器是(填写代号)_________________。
A.烧杯 B.量筒 C.1000 mL容量瓶 D.托盘天平E.药匙 F.500 mL容量瓶 G.胶头滴管 H.漏斗
除上述可使用的仪器,还缺少的仪器是_________ ,
(4)叙述定容过程中的操作___________________________________。
(5)要配制浓度约为2 mol·L-1 NaOH溶液100 mL,下列操作正确的是_____ 。
①称取8 g NaOH固体,放入250 mL烧杯中,用100 mL量筒量取100 mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解。
②称取8 g NaOH固体,放入100 mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL。
③称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加水至刻度线,塞好瓶塞,反复摇匀。
④用100 mL量筒量取40 mL 5 mol·L-1 NaOH,倒入250 mL烧杯中,再用同一量筒量取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中。
(6)下列操作导致所配溶液浓度偏高的是
A.称量时,左盘高,右盘低 B.定容时俯视容量瓶刻度线
C.原容量瓶洗净后没有干燥 D.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上期中考试化学试卷(解析版) 题型:选择题
能正确表示下列化学反应的离子方程式的是
A.实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O
B.饱和氢氧化钙溶液与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O
C.在氢氧化钡溶液中加入少量小苏打:Ba2++2OH-+2HCO3-=BaCO3 ↓+ CO32-+2H2O
D.NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第一次月考化学试卷(解析版) 题型:选择题
等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应。若生成硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐的物质的量浓度之比为
A.1:2:3 B.1:3:6 C.1:3:3 D.1:6:9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com