
可逆反应:2NO2 2NO+O2在定容密闭容器中
反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2 nmolNO2
②单位时间内生成n molO2的同时生成2 nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
安全是顺利进行实验的保障,下列实验处理或方法正确的是( )
A.含氯气的尾气用澄清石灰水吸收较好
B.把氢气和氯气混合光照制氯化氢
C.导管口点燃一氧化碳时也要验纯
D.重金属盐有毒,如果不慎食入氯化钡,喝入硫酸铜溶液即可
查看答案和解析>>
科目:高中化学 来源: 题型:
向一容积不变的密闭容器中充入一定量A和B,发生如下反应:
x A(g)+2B(s)  y C(g);△H <0在一定条件下,容器中 A、C的物质的量浓度 随时间变化的曲线如下图。请回答下列问题:
y C(g);△H <0在一定条件下,容器中 A、C的物质的量浓度 随时间变化的曲线如下图。请回答下列问题:
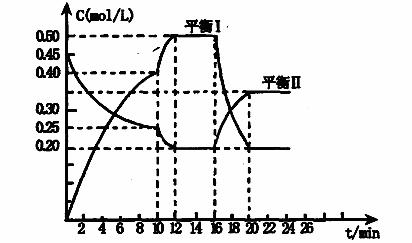
(1)用A的浓度变化表示该反应0~10min内的平均反应速率v(A)= ;
(2)根据图示可确定x:y= ;
(3)0~l0min容器内压强____ (填 “变大”,“不变”或“变小”)
(4)推测第l0min引起曲线变化的反应条件可能是 (填序号);第16min引起曲线变
化的反应条件可能是____ (填序号);
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(5)若平衡I的平衡常数为K1,平衡Ⅱ平衡常数为K2,则K1 K2(填“>”“=”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A. 常温下,0.1mol碳酸钠晶体中含有CO32-的个数为0.1 NA
B.标准状况下22.4 L H2O所含分子数为NA
C. 1L 0.5mol·L-1 CH3COOH溶液中,CH3COO-离子的个数为0.5NA
D. NO、NO2混合气体22.4L含有的氮原子数为NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
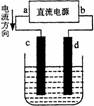
右图是电解CuCl2溶液的装置,其中c、d为石墨电极。
则下列有关的判断正确的是 ( )
A.a为负极、b为正极
B.a为阳极、b为阴极
C. 电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
按下图装置进行实验,并回答下列问题
 |
⑴锌极为__________极,电极反应式为_________________________
石墨棒C1为______极,电极反应式为________________________
石墨棒C2附近发生的实验现象为_______________________________
⑶当C2极析出224mL气体(标准状态)时,锌的质量减少_________g.
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家刚刚发现了某种元素的原子,1个该原子质量是a g,一个12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是( )
①该原子的相对原子质量为 ②m g该原子的物质的量为 mol
③该原子的摩尔质量是aNA g ④Wg该原子中含有 个该原子
个该原子
⑤由已知信息可得:
A.①②④ B.②③④ C.①②⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
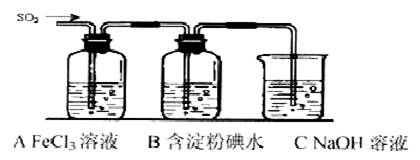
(1)SO2气体还原Fe3+反应的还原产物、氧化产物分别是 、
(填离子符号)。
(2)下列实验方案可以用于在实验室制取所需SO2的是 。
A.Na2SO3溶液与HNO3 B.硫在空气中燃烧 C.Na2SO3固体与浓硫酸
(3)装置C的作用是 。
(4)如果有280 mL SO2气体(已折算为标态)进入C装置中,则C中,50 mL
NaOH溶液的浓度至少为 mol/L才能达到目的。
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反
应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 ,原因是
(6)能表明I-的还原性弱于SO2的现象是 ,写出有关离子方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com