
【题目】由反应物X 转化为Y 和Z的能量变化如图所示.下列说法正确的是( ) 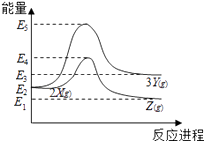
A.由X→Y反应的△H=E5﹣E2
B.由X→Z反应的△H>0
C.降低压强有利于提高Y的产率
D.升高温度有利于提高Z的产率
【答案】C
【解析】解:A.根据化学反应的实质,由X→Y反应的△H=E3﹣E2 , 故A错误;
B.由图象可知,反应物的总能量高于生成物的总能量,该反应为放热反应,即由反应的△H<0,故B错误;
C.根据化学反应2X(g)≒3Y(g),该反应是气体系数和增加的可逆反应,降低压强,平衡正向移动,有利于提高Y的产率,故C正确;
D.由B分析可知,该反应为放热反应,升高温度,平衡逆向移动,Z的产率降低,故D错误;
故选C.
【考点精析】掌握化学平衡状态本质及特征是解答本题的根本,需要知道化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】如图装置,试管中盛有水,气球a中盛有干燥的Na2O2颗粒,U形管中注有浅红色的水,将气球用橡皮筋紧缚在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是
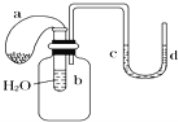
A. U形管内红色褪去
B. 试管内溶液变红
C. 气球a变瘪
D. U形管水位d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是( )
A.用KIO3氧化酸性溶液中的KI:5I﹣+IO3﹣+3H2O═3I2+6OH﹣
B.将过量SO2通入冷氨水中:SO2+NH3H2O═HSO3﹣+NH4+
C.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH﹣═NH3↑+H2O
D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3﹣═Ag++NO↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色稀溶液X中,可能含有如表所列离子中的某几种.取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(y)的关系如图所示.下列说法正确的是( )
阴离子 | CO32﹣、SiO32﹣、[Al(OH)4]﹣、Cl﹣ |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
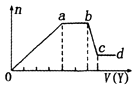
A.若Y是盐酸,则X中一定含有CO32﹣、SiO32﹣、[Al(OH)4]﹣和NH4+
B.若Y是NaOH溶液,则X中一定含有A13+、Fe3+、NH4+、Cl﹣
C.若Y是NaOH溶液,则ab段发生反应的离子方程式为:NH4++OH﹣═NH3↑+H2O
D.若Y是NaOH溶液,则X中的Al3+、Mg2+、NH4+物质的量之比为2:1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学利用图1所示实验装置进行NH3的制备、性质等实验. 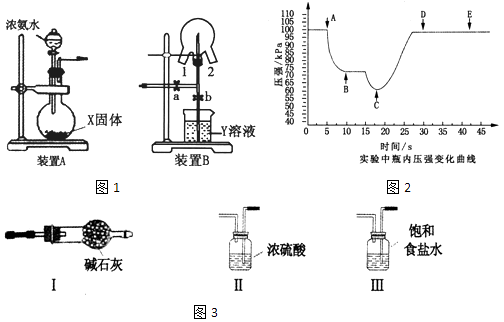
(1)装置A中的烧瓶内的X固体宜选用(填序号).
a.消石灰 b.氯化钙 c.五氧化二磷 d.生石灰
烧瓶中制取NH3的化学方程式为 .
(2)为制取干燥的氨气,可将装置A与下列装置如图3(填序号)进行连接.
(3)装置B可用于探究氯气与氨气的反应.实验时先通过三颈瓶瓶口1通入氨气,然后关闭b活塞,再通过瓶口2通入氯气.
①实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为 , 请设计一个实验方案鉴定该固体中的阳离子;
②实验完毕后,观察到三颈瓶内还有黄绿色气体,简述如何处理才能不污染环境 .
(4)可用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理:装置A与装置B相连,打开a,关闭b,开始实验,使三颈瓶内充满NH3 . 将吸有2mL H2O的胶头滴管塞进颈口1,通过颈口2将数据采集器的探头插入三颈瓶中.打开b,关闭a,挤压胶头滴管,进行喷泉实验,电脑绘制三颈瓶内气压变化曲线如图2.该图中点时喷泉最剧烈.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( ) 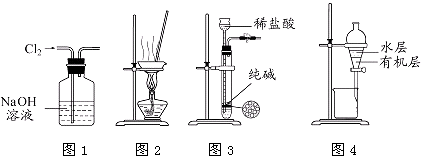
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)将稀盐酸逐滴滴入到含有酚酞的NaOH溶液中,可观察到的现象是 , 反应的离子方程式为:
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量.其热化学方程式为
(3)已知C的燃烧热△H=﹣393.5kJ/mol,则24g C在O2中完全燃烧生成CO2(g)放出的热量为kJ.
(4)工业上常用天然气作为制备CH3OH的原料.已知:
①CH4(g)+O2(g)=CO(g)+H2(g)+H2O(g)△H=﹣321.5kJ/mol
②CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+250.3kJ/mol
③CO(g)+2H2(g)=CH3OH(g)△H=﹣90.0kJ/mol
CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32﹣;⑦NO3﹣中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( ) 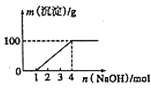
A.③⑤⑦
B.②③⑤⑦
C.①②③⑥⑦
D.①②③④⑤⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com