
将0.4mol丁烷完全燃烧后生成的气体全部缓慢通入1L 2mol/LNaOH溶液中,生成的 Na2CO3和NaHCO3的物质的量之比为 ( )
A.3:2 B.2:3 C.2:1 D.1:3
科目:高中化学 来源: 题型:
A+B→X+Y+ H2O(为配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1∶4.请回答:
(1)若Y是黄绿色气体,则Y的电子式是 ,该反应的化学方程式是
.
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是 .
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中.
①A元素在周期表中的位置是______(填所在周期和族);Y的化学式是______.
②含a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是______ mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,X、Y与Z不同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z.
(1)Q的最高价氧化物,其固态属于 分子 晶体,俗名叫 干冰 ;
(2)R的氢化物分子的空间构型是 正四面体 ,属于 非极性 分子(填“极性”或“非极性”);它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是 Si3N4 ;
(3)X的常见氢化物的空间构型是 三角锥型 ;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是  ;
;
(4)Q分别与Y、Z形成的共价化合物的化学式是 CS2 和 CCl4 ;Q与Y形成的分子的电子式是 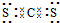 ,属于 非极性 分子(填“极性”或“非极性”).
,属于 非极性 分子(填“极性”或“非极性”).
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是 ( )



|


|
 C、a为正极,是碳棒,烧杯中的溶液为硫酸
C、a为正极,是碳棒,烧杯中的溶液为硫酸
D、b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应M+N→P,如果温度每升高10℃,化学反应速度增大为原来的3倍,在10℃时,完成反应10%需81min,则在30℃时完成反应10%需要时间为( )
A.27min B.9min C.13.5min D.3min
查看答案和解析>>
科目:高中化学 来源: 题型:
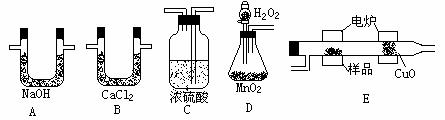 化学上常用燃烧法确定有机物的组成。这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下列装置是用燃烧法确定有机物分子式常用的装置。回答下列问题:
化学上常用燃烧法确定有机物的组成。这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下列装置是用燃烧法确定有机物分子式常用的装置。回答下列问题:
(1)产生的氧气按从左到右流向,所选装置的连接顺序为
(2)C装置中浓硫酸的作用是 ;
(3)D装置中MnO2的作用是 ;
(4)燃烧管中CuO的作用是 ;
(5)若准确称取0.90g样品(只含C、H、O三种元素中的两种或三种)经充分燃烧后,A管质量增加1.32g,B管质量增加0.54g,则该有机物的最简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
控制适当的条件,将反应Fe3++Ag═Fe2++Ag+设计成如图所示的原电池.下列判断正确的是( )
|
| A. | 反应开始时,石墨棒作阳极,银棒作阴极 |
|
| B. | 灵敏电流计的读数由小变大,再变小 |
|
| C. | 反应达化学平衡时,电流计读数最大 |
|
| D. | 反应达化学平衡时,在乙烧杯中滴入一定量的NaCl溶液,电流计指针又偏转 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.除去Cu2+中的少量Fe3+,可加入CuO
B.沸点:晶体硅 > SiO2 > SiCl4 > NaCl
C.Cu(NH3)42+中的配位键是由Cu2+提供孤对电子,NH3提供空轨道形成的
D.石油的分馏、煤的液化以及煤的干馏等生产过程中均只发生物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质分类正确的是 ( )
A.SO2、SiO2、CO均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、水玻璃、氨水均为混合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com