
| V |
| Vm |
| 11g |
| 44g/mol |
| 0.25mol×2 |
| 3 |
| 0.25mol×2 |
| 3 |
| 40 |
| 3 |
|
| 40 |
| 3 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、3.00g | B、3.43g |
| C、4.47g | D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、固体NaCl不导电,所以NaCl是非电解质 |
| B、NH3、CO2的水溶液的导电,所以NH3、CO2是电解质 |
| C、铜、石墨均能导电,所以它们都是电解质 |
| D、蔗糖在水溶液中或熔融时均不导电,所以是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述三个反应都有单质生成,所以都是置换反应 |
| B、氧化性由强到弱的顺序是KBrO3>KClO3>Cl2>Br2 |
| C、反应②中还原剂与氧化剂的物质的量之比为6:1 |
| D、反应③中1mol还原剂参加反应时氧化剂得到电子的物质的量为2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫元素的质量比为 4:5 |
| B、分子数之比为3:4 |
| C、原子总数之比为3:4 |
| D、质量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化碳增多使太阳辐射到地球表面的能量增多 |
| B、二氧化碳等气体能释放能量,使大气层的温度升高 |
| C、氟氯烃等大量排放,破坏臭氧层引起的 |
| D、二氧化碳、甲烷等温室气体产生温室效应,使大气温度升高,加速冰层融化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
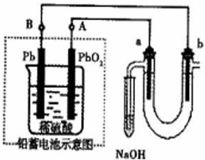 用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是 ( )(填序号)
用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是 ( )(填序号)| A、铅蓄电池负极的反应式为:Pb-2e-=Pb2+ |
| B、铅蓄电池放电时,B极质量减轻,A极质量增加 |
| C、铅蓄电池充电时,A极应与外电源负极相连 |
| D、电解苦卤水时,a电极首先放电的是Br- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com