
【题目】工业制硫酸中的一个反应:2SO2(g)+O2(g)![]() 2SO3(g),下列有关说法错误的是( )
2SO3(g),下列有关说法错误的是( )
A.在反应条件下,SO2不可能100%转化为SO3
B.达到平衡时SO2的浓度与SO3浓度相等
C.使用催化剂能加快反应速率
D.平衡后再升高温度平衡会改变
科目:高中化学 来源: 题型:
【题目】甲醇又称“木醇”或“木精”,沸点64.7℃,是无色有酒精气味易挥发的液体。甲醇有毒,误饮5~10mL能双目失明,大量饮用会导致死亡。甲醇是重要的化学工业基础原料和液体燃料,可用于制造甲醛和农药,并常用作有机物的萃取剂和酒精的变性剂等。
(1)工业上可利用CO2和H2生产甲醇,方程式如下:
CO2(g)+3H2(g)![]() CH3OH(l)+H2O (g) △H=Q1kJ·mol-1
CH3OH(l)+H2O (g) △H=Q1kJ·mol-1
又查资料得知:①CH3OH(l)+1/2 O2(g)![]() CO2(g)+2H2(g) △H=Q2kJ·mol-1
CO2(g)+2H2(g) △H=Q2kJ·mol-1
②H2O(g)=H2O(l) △H= Q3kJ·mol-1,则表示甲醇的燃烧热的热化学方程式为____。
(2)工业上可用CO和H2O (g) 来合成CO2和H2,再利用(1)中反应原理合成甲醇。某温度下,将1molCO和1.5molH2O充入10L固定密闭容器中进行化学反应:
CO(g)+H2O(g)![]() CO2(g)+H2(g) △H>0,当反应进行到10min时达到平衡,此时测得H2为0.6 mol。回答下列问题:
CO2(g)+H2(g) △H>0,当反应进行到10min时达到平衡,此时测得H2为0.6 mol。回答下列问题:
①0~10min内H2O(g)的平均反应速率为_________________。
②若想加快正反应速率的同时提高CO的转化率,可以采用的方法是__________。
a.升高温度 b.缩小容器的体积
c.增大H2O (g)的浓度 d.加入适当的催化剂
③若保持温度容积不变再向其中充入1molCO和0.5molH2O(g),重新达到化学平衡状态时,此时平衡混合气体中H2的体积分数为_____。
(3)甲醇燃料电池是符合绿色化学理念的新型燃料电池,下图是以甲醇燃料电池(甲池)为电源的电解装置。已知:A、B、C、D、E、F都是惰性电极,丙中为0.1 mol/L CuSO4溶液 (假设反应前后溶液体积不变) ,当向甲池通入气体a和b时,D极附近呈红色。回答下列问题:
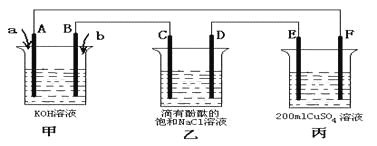
①a物质是__________, A电极的电极反应式为__________。
②乙装置中的总化学反应方程式为___________________。
③当乙装置中C电极收集到224mL(标况下)气体时, 丙中溶液的pH=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案不能达到实验目的的是
选项 | 实验方案 | 实验目的 |
A. | 向酸性 | 验证草酸具有还原性 |
B. | 向相同浓度的NaBr和KI溶液中分别滴加足量氯水,观察溶液颜色变化 | 比较溴元素和碘元素的非金属性强弱 |
C. | 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 | 研究温度对化学平衡的影响 |
D. | 将 | 制备硫酸镁晶体 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,室温下向盛有3.0mL NO的试管中缓缓通入1.5mL O2(所有气体的体积均在标准状况下测定)。
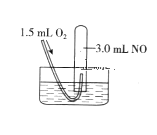
试回答下列问题:
(1)写出观察到的现象(可不写满,也可补充):
①__________;
②__________;
③__________。
(2)上述过程中发生反应的化学方程式有__________。
(3)最终试管中剩余的气体是__________,体积为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂为了综合利用生产过程中生成的CaSO4,与相邻的合成氨厂联合设计了以下制备(NH4)2SO4的工艺流程:
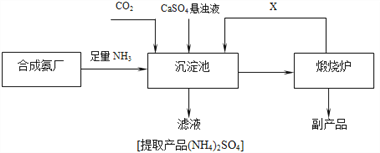
下列有关说法错误的是
A. 将滤液蒸干,即可提取产品(NH4)2SO4
B. 通入足量氨气使悬浊液呈碱性有利于CO2的吸收
C. 副产品是生石灰,X是CO2,其中CO2可循环利用
D. 沉淀池中发生的主要反应为CaSO4+CO2+2NH3+H2O![]() CaCO3↓+(NH4)2SO4,
CaCO3↓+(NH4)2SO4,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
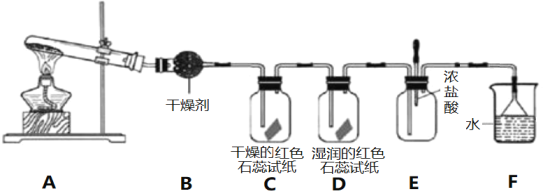
(1)B装置中的干燥剂是_________________(填“碱石灰”或“浓硫酸”)。
(2)C、D装置中试纸颜色会发生变化的是___________(填”C”或“D”)。
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到E装置中的现象是产生_____________(填”白烟”或“白雾”)。
(4)烧杯F中水的作用是________________________。
(5)欲制得标准状况下11.2 LNH3,至少需要Ca(OH)2的质量为____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中,能使电离平衡H2O![]() H+ + OH-正向移动且溶液呈酸性的是( )
H+ + OH-正向移动且溶液呈酸性的是( )
A. 向水中加入NaHSO4溶液 B. 向水中加入Al2(SO4)3溶液
C. 向水中加入Na2CO3溶液 D. 将水加热到100℃,使水的pH=6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近我国成功研制出高效电催化固氮催化剂Mo2N,如图所示,在0.1mol·L-1盐酸溶液中,在一定电压下具有较高的产氨速率和稳定的电流效率。下列判断错误的是
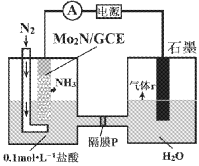
A. 石墨电极为阳极
B. P为阳离子交换膜
C. Mo2N/GCE电极区反应式为N2+6H++6e-=2NH3
D. 为提高溶液的导电性,可在石墨电极区加入适量的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体![]() 是一种黄色难溶于水的固体,受热易分解,是生产锂电池、涂料、着色剂以及感光材料的原材料。
是一种黄色难溶于水的固体,受热易分解,是生产锂电池、涂料、着色剂以及感光材料的原材料。
I、制备草酸亚铁晶体:
![]() 称取硫酸亚铁铵晶体
称取硫酸亚铁铵晶体![]() ,放入
,放入![]() 三颈烧瓶中,加入10滴左右
三颈烧瓶中,加入10滴左右![]() 溶液和
溶液和![]() 蒸馏水加热溶解;
蒸馏水加热溶解;
![]() 加入
加入![]() 饱和草酸溶液,加热搅拌至沸,停止加热,静置;
饱和草酸溶液,加热搅拌至沸,停止加热,静置;
![]() 待黄色晶体
待黄色晶体![]() 沉淀后倾析,洗涤,加入约
沉淀后倾析,洗涤,加入约![]() 蒸馏水搅拌并温热
蒸馏水搅拌并温热![]() ,静置,弃去上层清液,即得黄色草酸亚铁晶体。
,静置,弃去上层清液,即得黄色草酸亚铁晶体。
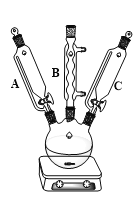
回答下列问题:
(1)仪器C的名称是_____________;仪器B的作用是_____________
(2)硫酸亚铁铵晶体用硫酸溶解的原因是 _____________________
II、探究草酸亚铁的纯度:
![]() 准确称取
准确称取![]() 草酸亚铁固体样品
草酸亚铁固体样品![]() 含有草酸铵杂质
含有草酸铵杂质![]() ,溶于
,溶于![]() 溶液中,在
溶液中,在![]() 水浴加热,用
水浴加热,用![]() 容量瓶配成
容量瓶配成![]() 溶液;
溶液;
![]() 取上述溶液
取上述溶液![]() ,用
,用![]() 标准溶液
标准溶液![]() 浓度为
浓度为![]() 滴定三次,平均消耗
滴定三次,平均消耗![]() ;
;
![]() 加入适量锌粉和
加入适量锌粉和![]() 溶液,反应一段时间后,取1滴试液放在点滴板上检验,至
溶液,反应一段时间后,取1滴试液放在点滴板上检验,至![]() 极微量;
极微量;
![]() 过滤除去锌粉,滤液收集在另一个锥形瓶中,将滤纸及残余物充分洗涤,洗涤液并入滤液中,再补充约
过滤除去锌粉,滤液收集在另一个锥形瓶中,将滤纸及残余物充分洗涤,洗涤液并入滤液中,再补充约![]() 溶液,继续用
溶液,继续用![]() 标准溶液
标准溶液![]() 浓度为
浓度为![]() 滴定至终点,共平行测定三次,平均消耗
滴定至终点,共平行测定三次,平均消耗![]() 。
。
回答下列问题:
(3)在![]() 中溶液中发生
中溶液中发生![]() ,还有另一氧化还原反应,写出其离子方程式_______________________,用
,还有另一氧化还原反应,写出其离子方程式_______________________,用![]() 标准溶液滴定至终点的现象是__________________。
标准溶液滴定至终点的现象是__________________。
(4)加入适量锌粉的目的是______________________________________;步骤![]() 中检验其中微量的
中检验其中微量的![]() 的试剂名称是______________溶液
的试剂名称是______________溶液
(5)计算![]() 固体样品的纯度为______________
固体样品的纯度为______________![]() 用含c、
用含c、![]() 、
、![]() 的式子表示,不必化简
的式子表示,不必化简![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com