
【题目】阿伏加德罗常数约为NA。下列叙述中正确的是 ( )
A. I L 0.1mol/L的FeCl3溶液中,H+的数目约为0.1NA
B. 1 mol金刚石中含有C-C键的数目为2NA
C. 7.8 g Na2O2中含有的阴离子数目约为0.2NA
D. 标准状况下,l L甲醇完全燃烧后生成的CO2分子个数约为(1/22.4)NA
【答案】B
【解析】
A.1L0.1mol/L的FeCl3溶液中n(FeCl3)=1L×0.1mol/L=0.1mol,Fe3+能发生一定程度的水解,但产生的H+的物质的量小于0.1mol,数目小于0.1NA,故A错误;B.金刚石晶体中每个C原子成4个C-C,故1个C-C键为2个C原子共用,故1mol金刚石含有2molC-C键,1mol金刚石中含有C-C键的数目为2NA,故C正确;C. 7.8g过氧化钠的物质的量为![]() ,Na2O2中含有的阴离子为O22-,O22-的物质的量为0.1mol,故含有含有的阴离子数目约为0.1NA,故C错误;D.甲醇是液体,不能利用气体摩尔体积22.4L/mol,1L甲醇的物质的量远远大于(1/22.4)NA,故D错误;本题选B。
,Na2O2中含有的阴离子为O22-,O22-的物质的量为0.1mol,故含有含有的阴离子数目约为0.1NA,故C错误;D.甲醇是液体,不能利用气体摩尔体积22.4L/mol,1L甲醇的物质的量远远大于(1/22.4)NA,故D错误;本题选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】铬元素及其化合物在生产、生活中具有广泛的用途。以某铬矿石(主要成分是Cr2O3,含Fe2O3、SiO2等杂质)为原料生产Cr2O3的流程如下:
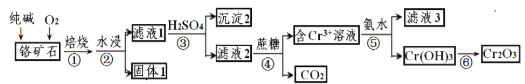
已知:2Cr2O3+4Na2CO3+3O2![]() 4Na2CrO4+4CO2,焙烧时SiO2也参与反应。
4Na2CrO4+4CO2,焙烧时SiO2也参与反应。
(1)Cr(OH)3和Al(OH)3性质类似,则Cr(OH)3与KOH反应的离子方程式为_________________;
(2)沉淀2的化学式为__________;
(3)步骤③中CrO42-转化成Cr2O72- ,写出其离子方程式____________________,硫酸能否换成盐酸并说明其理由___________________;
(4)滤液3中的主要溶质是两种盐,其化学式为__________________________;
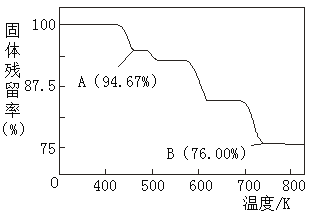
(5)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示,则B点时铬的氧化物化学式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6molW气体和0.5molX气体混合于2L密闭容器中,使它们发生如下反应:4W(g)+3X(g) ![]() 2Y(g)+nZ(g)。2min末已生成0.2mol Y,若测知以Z的浓度变化表示的反应速率为0.0025mol/(L·s),试计算
2Y(g)+nZ(g)。2min末已生成0.2mol Y,若测知以Z的浓度变化表示的反应速率为0.0025mol/(L·s),试计算
(1)前2min内用W的浓度变化表示的平均反应速率为_______________。
(2)2min末时X的浓度为_____________________________。
(3)化学反应方程式中n=_____________________________。
(4)2min末,恢复到反应前温度,体系内压强是反应前压强的__________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学将一定浓度NaHCO3溶液加入到CuSO4溶液中发现生成了沉淀。甲同学认为沉淀是CuCO3;乙同学认为沉淀是CuCO3和Cu(OH)2的混合物,他们设计实验测定沉淀中CuCO3的质量分数。
(1)按照甲同学的观点,发生反应的离子方程式为_____________________。
(2)两同学利用下图所示装置进行测定:

①在研究沉淀物组成前,须将沉淀从溶液中分离并净化。具体操作依次为过滤、洗涤、干燥。
②装置E中碱石灰的作用是__________________。
③实验过程中有以下操作步骤:
a.关闭K1、K3,打开K2、K4,充分反应
b.打开K1、K4,关闭K2、K3,通入过量空气
c.打开K1、K3,关闭K2、K4,通入过量空气
正确的顺序是____(填选项序号,下同)。若未进行步骤____,将使测量结果偏低。
④若沉淀样品质量为m g,装置D质量增加了n g,则沉淀中CuCO3的质量分数为____。
(3)丙同学认为还可以通过测量CO2的体积并测量____来测定沉淀中CuCO3的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要证明某溶液中不含Fe3+而可能含有Fe2+进行如下实验操作时最佳顺序为
①加入足量氯水 ②加入足量KMnO4溶液③ 加入少量KSCN溶液
A.①②B.③②C.③①D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.2 mol·L-1NaOH溶液480 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。

(2)下列有关容量瓶使用方法的操作中,错误的是_______。
A.使用容量瓶之前应检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶中直至与刻度线齐平
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒,摇匀
(3)在配制NaOH溶液时:
①根据计算用托盘天平称取NaOH的质量为________g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________(填“>”“<”或“=”)0.2 mol·L-1;
③若NaOH固体溶解后立即移入容量瓶→洗烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度________(填“>”“<”或“=”)0.2 mol·L-1。
(4)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________(计算结果保留一位小数)mL;
②如果实验室有15 mL、20 mL、50 mL量筒,应选用______mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是___________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是
A. c(Fe2+) =1mol·L1的溶液中:K+、NH4+、MnO4、SO42
B. ![]() =1×10-13 mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
=1×10-13 mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
C. 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42-
D. ![]() =1×10 12的溶液中:K+、Na +、CO32-、NO3-
=1×10 12的溶液中:K+、Na +、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚异戊二烯橡胶( )具有与天然橡胶相似的化学组成、立体结构和力学性能,具有良好的强度、黏性和弹性等,其合成路线如下图:
)具有与天然橡胶相似的化学组成、立体结构和力学性能,具有良好的强度、黏性和弹性等,其合成路线如下图:

已知:
① ;
;
②同一碳原子上有两个碳碳双键时分子不稳定。
(1)A既能使酸性KMnO4溶液褪色,也能使溴的四氯化碳溶液褪色,则A的化学名称是__________,该物质中含有的官能团名称是______________。
(2)![]() 和氧气作反应物,温度为110℃时除生成B外,还生成一种副产物F,其分子式为C6H6O,该物质的水溶液遇FeCl3溶液显紫色,那么物质F不可能发生的反应类型是_________。
和氧气作反应物,温度为110℃时除生成B外,还生成一种副产物F,其分子式为C6H6O,该物质的水溶液遇FeCl3溶液显紫色,那么物质F不可能发生的反应类型是_________。
a.加成反应 b.取代反应 c.消去反应 d.缩聚反应
(3)写出合成路线图中有机化合物C的结构简式___________________。
(4)写出D生成E的化学反应方程式_____________。
(5)D的同分异构体中能发生银镜反应的共有______种,其中核磁共振氢谱有五种不同化学环境的氢,且峰面积比为3:3:2:1:1是______________(写结构简式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com