
| A、离子化合物中一定含有离子键 |
| B、单质分子中均不存在化学键 |
| C、离子化合物中一定不含共价键 |
| D、含有共价键的化合物一定是共价化合物 |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
| A、HF、HCI、HBr、HI的热稳定性依次减弱 |
| B、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| C、F2、C12、Br2、I2的熔、沸点逐渐升高 |
| D、Li、Na、K、Rb 的熔点逐渐降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入金属镁能产生H2的溶液中:Na+、Fe2+、SO42-、NO3- |
| B、含有大量Fe2+的溶液中:K+、Mg2+、ClO-、SO42- |
| C、能使Al3+生成沉淀的溶液中:NH4+、Na+、SiO32-、HCO3- |
| D、水电离产生的c(OH-)=1×10-10mol/L的溶液中:Al3+、SO42-、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水中一水合氨的电离方程式:NH3?H2O═NH4-+OH- | |||
| B、氢氧化钡溶液跟稀硫酸反应的离子方程式:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |||
C、苯和硝酸反应的化学方程式: +HNO3 +HNO3
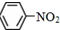 +H2O +H2O | |||
| D、25℃、101 kPa时,1 g甲醇完全燃烧生成CO2和液态水放出22.68 kJ的热量,所以反应物的能量低于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 物质 | 被选出的物质 | 选择依据 |
| 1 | O2、H2、Cl2、N2 | ||
| 2 | Fe、Na、Al、C | ||
| 3 | NaOH、CO2、H2SO4、Fe2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com