
| A、HF、HCI、HBr、HI的热稳定性依次减弱 |
| B、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| C、F2、C12、Br2、I2的熔、沸点逐渐升高 |
| D、Li、Na、K、Rb 的熔点逐渐降低 |


科目:高中化学 来源: 题型:
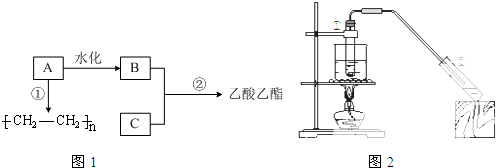
查看答案和解析>>
科目:高中化学 来源: 题型:
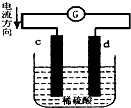 如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c、d为两个电极.则下列有关的判断不正确的是( )
如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c、d为两个电极.则下列有关的判断不正确的是( )| A、d为负极,发生氧化反应 |
| B、c为锌片,电池工作时,溶液中SO42-向c移动 |
| C、电池工作的过程中,d电极上产生大量的气泡 |
| D、电池工作的过程中,溶液中SO42-浓度基本不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子化合物中一定含有离子键 |
| B、单质分子中均不存在化学键 |
| C、离子化合物中一定不含共价键 |
| D、含有共价键的化合物一定是共价化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com